第八单元 金属和金属材料 综合评估
http://www.newdu.com 2025/11/06 12:11:29 人民教育出版社 佚名 参加讨论
第八单元 金属和金属材料 综合评估 火眼金睛 1.下列关于铁的说法中,错误的是( ) A.铁在潮湿的空气中容易生锈 B. 铁在空气中容易燃烧 C.铁具有可变化合价 D.铁是由铁原子直接构成的 2. 某些化学小组设计了验证Fe、Cu、Ag的金属活动性顺序的四种方案,各个方案选用的试剂如下,其中不可行的是( ) A.Fe、CuSO4溶液、Ag B.FeCl2>溶液、Cu、AgNO3溶液 C.Ag 、CuSO4溶液、FeSO4溶液 D. Fe、Cu、AgNO3溶液、盐酸 3.金属插入溶液中,溶液质量会增加的是( ) A.锌片插入硫酸铜溶液中 B.铁片插入硫酸铜溶液中 C.铜片插入硝酸银溶液中 D.铜片插入硫酸铝溶液中 4.下表中列出了几种物质的熔点(在标准大气压下)
据此判断下列说法中正确的是( ) A.铜球吊入铁水中不会熔化 B.水银温度计可测量零下40 ℃的气温 C.用钨制成的灯丝不易熔化 D.用石墨作灯丝更好 5.社会上一些不法分子以铜锌合金(金黄色,俗称黄酮)假冒黄金进行诈骗活动。为了鉴别黄酮和黄金,下列方法可行的是( ) A. 观察颜色 B.称取质量 C.用磁铁吸引 D.插入稀盐酸中 6.依据反应x+C  2y和Fe2O3+3y 2y和Fe2O3+3y 2Fe+3x,推断x和y各表示( ) 2Fe+3x,推断x和y各表示( )A.CO和CO2 B. CO2和CO C.H2O和CO D. CO2和H2 7.表示两个亚铁离子的符号是( ) A.2Fe B.2Fe2+ C.2Fe3+ 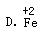 8.往CuO和Fe的混合粉末中,加入一定量的稀硫酸,并微热,当反应停止时,滤出不溶物,并向滤液中插入一铁钉,片刻后取出,发现铁钉无任何变化。则下面结论正确的是(已知:CuO+H2SO4===CuSO4+H2O( ) A.不溶物一定是Cu,不含Fe B.不溶物一定是Fe,不含Cu C.不溶物一定含有Cu,也可能含有Fe或CuO D.溶液中一定含有FeSO4和CuSO4,不含有H2SO4 9.除去硫酸亚铁溶液中的少量硫酸铜,应选用的试剂是( ) A.盐酸 B.铁粉 C.碳粉 D.氢气 10.下列说法中,错误的是( ) A.铝可作制造汽车、飞机的材料 B.铜在国防工业中用于制造枪弹、炮弹 C.锌常用作干电池的正极 D.钢的性能比生铁的性能优越 11.下了反应中,不属于置换反应的是( ) A.C+2CuO2  Cu+CO2↑ B. CO+CuO Cu+CO2↑ B. CO+CuO Cu+CO2 Cu+CO2C.2Al+3H2SO4===Al2(SO4)3+3H2↑ D. C+H2O  CO+ H2 CO+ H212. Fe、Fe2+、Fe3+三种粒子具有相同的( ) ①质子数 ②中子数 ③核外电子数 ④化学性质 A.①② B. ②④ C. ①③ D. ②④ 13.下列有关物质的颜色中,不正确的是( ) A.氯化亚铁溶液是浅绿色的 B.硫酸铜溶液是蓝色的 C.二氧化锰粉末是黑色的 D.纯净的铁锭是黑色的 14.下列物质中,不能有金属跟盐酸反应来生成的是( ) A.氯化锌 B.氯化镁 C.氯化铁 D.氯化亚铁 15.铁的某种化合物中,铁元素与硫元素的质量之比为7:8,则该化合物中铁元素与硫元素的原子个数之比是( ) A.1:2 B.2:1 C.3:2 D.2:3 画龙点睛 1.盛放在油罐车内的石油产品振荡可以产生静电,容易引起火灾,所以在油罐车尾部有一条拖地铁链,这是利用能__________的性质。 2.通过研究性学习,对钢铁制品锈蚀条件的研究,你得出的钢铁制品锈蚀条件是:__________________。防锈蚀的具体方法有(人举两例)______________________________________。 3.我国从西汉时期就开始炼铜,方法实现用硫酸和氧化铜反应生成硫酸铜和水,再用铁置换出铜,称为湿法炼铜。 (1) 写出上述两步反应的化学方程式。 ______________________________________________________; (2) 第二步反应的主要现象有: ______________________________________________。 4.某化工厂排出的废液中含有AgNO3、Zn(NO3)2和Cu(NO3)2三种物质。为了分离并回收金属银和铜,化学课外小组的同学设计了如下实验方案: 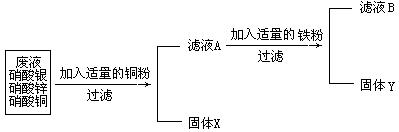 根据实验方案填空。 固体x是______,固体y是______,滤液B是________。 计算小擂台 1、把铁片放入硫酸铜溶液中,过一段时间后取出,在铁片上覆盖了12.8 g铜,求消耗铁片多少克?  2、有含杂质的氧化铁样品(杂质不参加反应),为了测定该样品中氧化铁的质量分数,某同学称取该样品10 g,并用下图所示的装置进行实验,得到如下两组数据: 2、有含杂质的氧化铁样品(杂质不参加反应),为了测定该样品中氧化铁的质量分数,某同学称取该样品10 g,并用下图所示的装置进行实验,得到如下两组数据:
试回答:(1)你认为,应当选择 组的数据来计算样品中的氧化铁的质量分数,计算的结果是 。 (2)这位同学所用装置的不足之处是 。 (责任编辑:admin) |
- 上一篇:课题1 常见的酸和碱 课后沟通
- 下一篇:弱酸性洗发剂能减少皱纹