2013年中考化学试题汇编——金属和金属材料(四)
http://www.newdu.com 2025/12/22 12:12:25 人民教育出版社 佚名 参加讨论
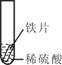
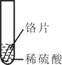
2013年中考化学试题汇编——金属和金属材料(四) 山东省微山县鲁桥一中 山东省微山县鲁桥一中 黄尊英 71.(2013.南京市)铁是应用最广泛的金属。 (1)写出铁丝在氧气中燃烧的化学方程式 。 (2)新型材料纳米级Fe粉能用作高效催化剂。实验室采用还原法制备纳米级Fe粉,其流程如下图所示: 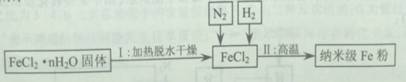 ①纳米级Fe粉在空气中易自燃。实验中通入N2的目的是 。 ②写出Ⅱ中H2还原FeCl2置换出铁的化学方程式 。 72.(2013.资阳市)向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有 ;氧化铜与稀硫酸反应的化学反应方程式为 。实验室用浓硫酸配制一定量的稀硫酸,正确操作是将 ,并不断搅拌。 73.(2013.潍坊市)铁及其化合物在生活生产中有重要的应用。请回答下列问题: (1)在盛有氧气的集气瓶中点燃细铁丝发生剧烈燃烧的化学方程式是 , 为防止集气瓶破裂,常采取的措施是 。 (2)已知铁能与氯化铁反应生成氯化亚铁。将生锈的铁钉(铁锈的主要成分是Fe2O3)放入盐酸中,充分反应后有铁剩余,写出发生置换反应的化学方程式 , 溶液中的金属阳离子是 (用符号表示)。 (3)高炉炼铁中,焦炭的作用是 (用化学方程式表示)。 (4)把铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后有固体剩余。下列说法正确的是 (填写字母序号)。 A.剩余固体肯定含有银 B.剩余固体肯定是银和铜 C.反应后溶液中一定有Fe2+ 和Cu2+ D.反应后溶液中可能含有Ag+ 和Cu2+ 74.(2013.资阳市)事物都具有两面性。如:CO可作冶金工业原料,却对人体健康有害;O2可用于急救病人,维持生命活动需要,却参与钢铁的锈蚀过程。 (1)写出高炉炼铁中CO还原氧化铁的化学反应方程式: ;煤气中毒是因为CO与血液中 结合,造成人体缺氧。 (2)钢铁制品在 中易生锈;钢和生铁都是铁与 元素形成的合金,由于该元素含量的不同,使得钢和生铁的坚韧性有较大差异。 75.(2013金华)某同学为比较镁和铝的金属活动性强弱,将两块表面积相同并除去氧化膜的镁条、铝条分别与相同体积、相同质量分数的稀硫酸反应,测定两种金属与稀硫酸反应得到相同体积氢气所需要的时间。 (1)实验前需用98%的浓硫酸配制10%的硫酸溶液。现有烧杯、玻璃棒、 胶头滴管,还需要的仪器有 。 (2)利用图甲中A、B仪器可以组装一套实验室测量取氢气体积的装置,该装置导管的连接顺序是 。 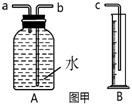 (2)图乙中量气管和水准管也可以用来测量氢气体积,为了准确地测量氢气体积,在读取量气管中液面读数的过程中,应注意 (填字母编号)。 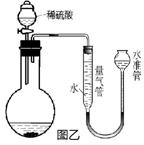 A.读数时视线与凹液面最低处相平 B.读数前应上下移动水准管,待两管液面相平再读数 C.保持水准管静止,待水准管中液面不再上升时再读数 76.(2013.泸州市)早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空: 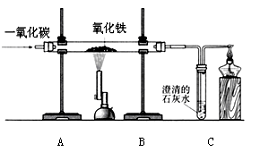 (1)A中观察到的现象是 。写出CO还原Fe2O3的化学方程式 ; (2)实验中盛澄清石灰水的试管中可观察到的现象是 ; (3)右边导气管口放置点燃的酒精灯的目的是 。 77.(2013.吉林省)2013年中央电视台举办的“3.15”晚会,曝出某品牌金饰品掺假的事件,引起同学们的好奇。某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动。 【提出问题】 (1)怎样鉴别真假黄金? (2)怎样确定钯的金属活动性? 【查阅资料】 (1)假黄金通常是黄铜(Cu-Zn合金); (2)钯(Pd)呈银白色,有金属光泽,可用作饰品。 【实验药品】 钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液 【实验探究】 (1)鉴别黄金样品的真假 取黄金样品于试管中,滴加稀盐酸后,观察到黄金样品表面有气泡产生,该气体是 ,说明此样品为 .(选填“真”或“假”)黄金。 (2)探究钯的金属活动性 依据生活经验,同学们猜想钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
初步得出结论:钯、银、铂的金属活动性由强到弱的顺序为 。 【废液处理】 (1)转化成沉淀。小组同学将所有液体倒入废液缸中,出现白色沉淀。写出产生该现象的化学方程式 .(写出一个即可); (2)通过科学合理的方法进一步回收金属钯。 78. (2013连云港) 某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你一起对此展开探究。 【设计方案】甲同学利用氢气还原氧化铜的原理和下图装置及药品进行实验(操作规范)。装置A中发生反应的化学方程式为 ,洗气瓶B中浓硫酸的作用为 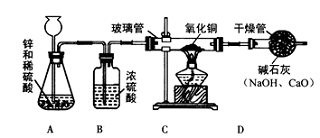 【实验探究】当玻璃管中固体由黑色转变为红色时,实验测得:①装置C的玻璃管和其中固体的总质量在反应后减少了1.6g;②装置D的干燥管和其中物质的总质量在反应后增加了1.82g,用此数据算得水中H、O元素的质量比为 ,而由水的化学式算得H、O元素的质量比为 。 【分析交流】针对上述结果与理论值有偏差,乙同学认为:该装置存在缺陷,此观点得到了大家的认同,你对此改进的方法是 (假设生成的水完全被D中碱石灰吸收,装置内空气中的水蒸气、CO2忽略不计)。小组同学用改进后的装置重新实验得到了正确结果。 【意外发现】丙同学不小心将反应后的少量红色固体a洒落到多量稀硫酸中了,发现除了有红色固体b以外,溶液的颜色由无色变为蓝色。 【提出问题】铜与稀硫酸是不反应的,这里溶液的颜色为什么会变蓝呢? 【查阅资料】①CuO被还原的过程中会有Cu2O生成,Cu2O也能被还原在Cu; ②Cu2O固体是红色的,它一稀硫酸的反应为: Cu2O+H2SO4=CuSO4+Cu+H2O. 【得出结论】红色固体a中含有Cu2O。 【分析交流】红色固体a中含 有Cu2O是否会影响水组成的测定结果 (填“影响”或“不影响”)。 【提出猜想】针对红色固体a的成分,小组同学提出猜想①是:Cu2O和Cu;猜想②是: 【拓展探究】丁同学利用改进后的装置及药品重新实验,通过测量反应前后固体质量的方法去确定哪种猜想成立,他已称得:①玻璃管的质量;②反应前红色固体a和玻璃管的总质量,完全反应后,你认为他还需要称量 的质量。 【教师点拨】称取一定质量的红色固体a与足量的稀硫酸充分反应后,经过滤、洗涤、干燥后再称量红色固体b的质量,也可以确定哪种猜想成立。 【定量分析】小组同学再次实验,他们开始称取质量为3.6g的红色固体a,与足量的稀硫酸完全反应后得到红色固体b为2g 。假如3.6g红色固体a都是Cu2O,请你计算出生成铜的质量(利用Cu2O+H2SO4=CuSO4+Cu+H2O.进行计算,写出计算过程);然后,通过与实际得到的固体2g进行比较,判断猜想 成立(填①或②)。 79.(2013.广州市)(5分)将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到约800℃,得到一种锌和铜的合金——黄铜,外观似黄金但质地坚硬。(提示:ZnCO3 ZnO + CO2↑) (1)黄铜是金属材料吗?___________(填“是”或“不是”)。 (2)写出其中赤铜和木炭粉反应的化学方程式__________________________________。 (3)若原料中含25吨ZnCO3 ,充分反应后,理论上所得黄铜中锌的质量为______吨。 80.(2013.娄底市)小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。 【知识回放】 金属活动性顺序:K Ca Na Mg Al Zn Sn Pb(H) Hg Ag Pt Au,请你在横线上填写对应金属的元素符号。 【作出猜想】 猜想1.Cr>Fe>Cu; 猜想2. Fe>Cu >Cr; 猜想3.你的猜想是 。 【查阅资料】 (1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。 (2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。 【设计与实验】 小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
【结论与解释】 (1)小聪得到的结论是猜想 正确。 (2)实验前用砂纸打磨金属片的目的是 。 【知识运用】 将铬片投入FeSO4溶液中,反应 (填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式 。 参考答案: 71.(1)3Fe +2O2 ② H2 + FeCl2 72.铜 CuO + H2SO4== CuSO4 + H2O 将浓硫酸沿着容器壁慢慢地注入盛有水的烧杯中 73.(1)3Fe +2O2 (2)Fe + 2HCl == FeCl2 + H2↑ Fe3+ (3)C + O2 (4)A D 74.(1)3CO+ Fe2O3 (2)潮湿的空气 碳 75.(1)量筒 (2)b接c (3)AB 76.(1)红棕色变成黑色 ,3CO+Fe2O3 (2)石灰水变浑浊 (3)燃烧多余的CO(或处理尾气等) 77.【实验探究】(1)氢气 假 (2)无明显现象 强 银>钯>铂 【废液处理】(1)2AgNO3 + PdCl2 = Pd (NO3)2 + 2AgCl↓ 78.【设计方案】Zn + H2SO4 == ZnSO4 + H2↑ 吸收水蒸气或干燥氢气 【实验探究】11:8 1:8 【分析交流】在D装置后,再连接一个盛碱石灰的干燥管,防止空气中的水蒸气和CO2加入D装置。 【分析交流】不影响 【提出猜想】Cu2O 【拓展探究】反应后红色固体和玻璃管的总质量 【定量分析】猜想①成立 解:设生成铜的质量为x Cu2O + H2SO4= CuSO4 + Cu + H2O 144 64 3.6g x X=1.6g 由于1.6g<2g 因此红色固体a中含有Cu2O和 Cu 79.(1)是 (2)2Cu2O + C 80.【知识回放】Fe .Cu 【作出猜想】Fe>Cr>Cu 【设计与实验】无明显现象发生(或无气泡生成,溶液也不变色) 【结论与解释】 1 除去金属表面的氧化膜,利于反应 【知识运用】 能 Cr+FeSO4=Fe+CrSO4 (责任编辑:admin) |
- 上一篇:《金属和金属材料》单元测试
- 下一篇:第八单元 金属和金属材料 综合评估