自然界的水 知识拓展运用
http://www.newdu.com 2025/12/14 11:12:26 人民教育出版社 佚名 参加讨论
自然界的水 知识拓展运用 湖北省宜昌市教育教学研究中心 刘四方 (一)化学与生产、生活  例1.(2007·福建福州新课程卷)用分子观点解释右图漫画中小女孩的话,正确的是D 例1.(2007·福建福州新课程卷)用分子观点解释右图漫画中小女孩的话,正确的是D A.分子质量小 B.分子间有间隔 C.分子体积小 D.分子在不断运动 【解析】此题考查学生运用分子的性质解释实际生活现象的能力。解答此题的关键在于如何从分子的诸多性质中寻求符合题意的答案。本题四个选项都是分子的性质,具有一定的迷惑性。小女孩被动吸烟,是因为烟雾扩散到空气中使小女孩嗅到烟味,说明分子在不断运动,不断地扩散。 【答案】D 【点评】在运用分子的性质分析实际生活中观察到的一些现象时,一定要将分子的性质和生活现象“对号入座”,紧紧抓住问题的核心指向,注意题目的意图和侧重点。 (二)化学与科技前沿 例2. (2007苏州市中考试题)试根据以下有关水的叙述填空。 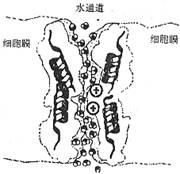 (1)假设水是由单个自由的水分子构成,按理论计算,常压下水的熔点是-110 ℃,沸点是-85 ℃;而实际上水的熔点是______℃,沸点是_______℃。实验证明,物质随分子质量的增大,其熔点、沸点随之升高。因此通常情况下,水是以_______[选填“单个分子”或“分子簇”(多分子集合体)]的形式存在。 (1)假设水是由单个自由的水分子构成,按理论计算,常压下水的熔点是-110 ℃,沸点是-85 ℃;而实际上水的熔点是______℃,沸点是_______℃。实验证明,物质随分子质量的增大,其熔点、沸点随之升高。因此通常情况下,水是以_______[选填“单个分子”或“分子簇”(多分子集合体)]的形式存在。(2)人剧烈运动大量出汗后,体内细胞需补充水。水分子进出细胞的原理如图1所示,水分子通过水通道蛋白膜时,由于通道中央存在的_______电荷,可将水中含有的阳离子(例如______离子)弹开,阻止了阳离子通过通道,使水分子在每个通道里能以每秒约10亿个分子的速度通过。 【解析】本题从考查水的物理性质入手,通过信息和图示来表达水在人的生理活动中的重要作用,同时又渗透有关物理知识。体现了学科之间相互融合、相互渗透的思想。(1)中解题的关键是要能对照假设中的理论计算“常压下水的熔点是 【答案】(1)0;100;分子簇(多分子集合体)。(2)正; 【点评】本题以水为载体,以最新的科技前沿信息为背景设计试题。情景新,知识活,起点高,落点低。问题的答案往往就蕴含在题给信息中,只要认真审题,领会题给信息,即可迎刃而解。 (三)开放性题 例3、(2007·黑龙江绥化市)学习水的组成这一课题后,同学们己经知道水在通电的条件下能生成氢气和氧气。某研究性学习小组同学对电解水的实验很感兴趣,很想通过实验验证这一结论。于是在征得老师同意后进行实验,实验记录如下:
电解水生成氢气和氧气的理论体积比是多少? 如果你是这次实验的参与者、请认真分析实验数据,你会发现什么问题? 推测产生这一间题的可能原因。 【解析】电解水的实验在课堂上都演示过,但对实验中的反常现象的分析往往忽略。第1问属于记忆性知识,如果电解产生的氢气和氧气没有任何损耗,理论上二者体积之比为2:1。分析表格中每一组数据,却发现H2和O2体积之比都大于2:1。说明生成的氧气被消耗了一部分,是什么原因造成了氧气的被消耗?再分析实验环境,生成的气体与水要充分接触,由此可以猜想可能是生成的氧气比氢气在水中的溶解能力大一些。另外,由于氧气化学性质比较活泼,还有可能生成的氧气与电极材料发生化学反应,消耗了一部分。 【答案】氢气和氧气的理论体积比为2:1; 发现的问题:氢气和氧气实际的体积比和理论体积比不符;(或:电解水负极与正极产生的气体体积比与理论体积比不相等,大于2:1;从第四分钟起,每两分钟内负极与正极生成气体的体积比与理论体积比相等。) 可能原因为:氧气在水中的溶解度比氢气在水中的溶解度大。(或:氧气比氢气易溶于水;生成的氧气与电极反应) 【点评】本题是一道表格数据型信息题。答案具有开放性。要求学生仔细分析表格中的数据,对比分析,发现问题。分析数据时有直接分析和间接分析,前者直接从已给数据中发现问题,后者则是对数据重新进行处理(如相减)得出新的数据后发现新的问题。在分析生成的氧气被消耗时,可以从物理消耗(溶解)和化学消耗(反应)上分别予以考虑。 (四)探究题 例4.(2007·广东韶关市新课程卷)去年,我市遭遇了超百年一遇的特大洪灾,在洪水面前,小敏同学利用课堂上学会的污水处理知识,对所取的洪水进行了净化处理,解决了家中的暂时用水问题。 (1)用纱布滤去水中的泥沙,她采用的是混合物分离中的__________操作。 (2)若经过操作(1)后的水显弱碱性,小敏可利用家中的(填序号)____将该水调至中性。 A. 白糖 B.食盐 C.食醋 D.白酒 (3)[发现问题]:小敏发现经过操作(1)后的水仍然浑浊,便在浑浊的水中加入适量的明矾,通过搅拌、静置后,发现水变得澄清了。 [查阅资料]:明矾[化学式:KA1(SO4)2·12H2O]是一种常见的净水剂,它在水中离解出的离子主要有K+、A13+、SO42- 。 [提出猜想]:明矾中哪一种离子有净水作用 小敏进行了如下实验,请填写表中空白:
(4)小敏实验方案不完善,需要对方案进行补充完善,请你把补充方案中要达到的目的和所使用的试剂填入下表。
【解析】第(1)问用纱布滤去水中的泥沙,是将固体物质和液体分离开来,采用的是过滤操作。要将过滤后水的弱碱性调至中性,应该加入一种酸,使之发生酸碱中和。题给四种物质中只有食醋显酸性。第(3)问是一道“发现式”的探究性试题。题目所给的信息是明矾溶于水后能离解出三种粒子K+、A13+、SO42-,是其中的哪一种粒子具有净水作用呢?小敏首先在一杯浑浊的水中加入少量KCl,静置,KCl在水中能提供K+和Cl-,结果是烧杯中的水仍然浑浊,由此说明K+和Cl-都没有净水作用。这实际上是采用了一种逐一排除的方法。第二次用Al2(SO4)3来检验,烧杯中的水变澄清,说明A13+和SO42-中有—种或两种有净水作用。接下来的实验方案的设计就是选定两种物质,一种含A13+,另一种含SO42-,而选定的这两种物质中的另一种离子不应该具有净水作用。结合前面已做过的实验,选定的物质应该是AlCl3和K2 SO4。 【答案】(1)过滤 (2)C (3)杯中的不仍然浑浊 Al3+和SO42-:—种或两种有净水作用 (4)
【点评】对于“发现式”探究性试题,解题时要利用已学知识进行整理和发现。其思维策略是:第一,要认真分析题给信息,确定欲探究的规律;第二,要对题中的文字信息、表格全方位地进行对比分析,发现具有普遍性的结论;第三,把自己通过分析比较得出的规律性结论与所给信息加以对照,最终得出正确的结论。另外,设计对比实验,控制变量,运用排除法,非此即彼,都是最常用的实验方法。 (五)综合题 例5、 (2007·江苏常州市)水是生命之源,万物之基,是人类最宝贵的自然资源。我国规定水质必须在感官性指标、化学指标、病理学指标等方面达标方可以成为生活饮用水。 (1)感官性指标的主要要求为:①不得呈现异色;②不得有异嗅异味;③不得含有肉眼可见物;④水应澄清透明。净化水时,前两个指标可以利用 的吸附作用(填物质名称)而达到;后两个指标可以通过加入混凝剂反应、沉降,然后通过 (填操作名称)而达到。 (2)化学指标中含有液体的pH和硬度两项。 ①测定溶液pH的方法是: 。 ②日常生活中如何区分硬水与软水?请简述实验步骤与现象: 。 (3)病理学指标中对铬、铅等重金属离子的含量有严格的限制。这是因为: 。 【解析】水的净化方法主要有吸附、过滤等。利用活性炭的吸附作用可以除去水中的色素和异味,是物理吸附,发生的是物理变化。过滤是将液体中的不溶性固体和液体分离的操作。第(1)问就不难得出正确答案。测定溶液pH的方法有很多种,如使用pH试纸或pH计等。生活中区分硬水与软水通常有两种方法,一种是加肥皂水后振荡观察产生泡沫的多少,另一种是取等量液体,煮开一段时间后观察水垢的多少。重金属离子有毒,工业废水中重金属离子应该进行净化处理达标后再排放,否则会影响人体健康。 【答案】(1)活性炭 过滤 (2)①pH试纸或pH计或酸度计。 ②在水中加入肥皂水搅拌,如泡沫较少,形成较多白色垢状物则为硬水,否则为软水。 (3)重金属离子会使人体蛋白质变性而造成中毒。 【点评】本题将水的净化、溶液pH的测定、硬水和软水的区分及重金属离子的危害等知识综合起来进行考查。体现了知识的综合性。复习时,要联系前后知识、新旧知识有机结合起来解决实际问题。 (责任编辑:admin) |
- 上一篇:物质构成的奥秘 能力提高
- 下一篇:化学实验基本操作总复习