物质构成的奥秘 能力提高
http://www.newdu.com 2025/12/09 01:12:08 人民教育出版社 佚名 参加讨论
物质构成的奥秘 能力提高 知识梳理 1.原子结构 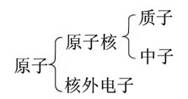 核电荷数=质子数=核外电子数 2.物质的构成和物质组成的表示 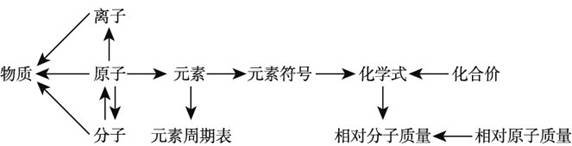 3.元素原子结构、元素分类和性质
中考链接 【例题1】(2005·山东省烟台市)科学家设想宇宙中可能存在完全由反粒子构成的反物质;正反粒子相遇会湮灭并释放出巨大的能量,在能源研究领域中前景可观。正电子、负质子等都是反粒子,它们跟通常所说的电子、质子相比较,质量相等但电性相反。请你推测,反氢原子的结构可能是( ) A.由1个带正电荷的质子和1个带负电荷的电子构成 B.由1个带负电荷的质子和1个带正电荷的电子构成 C.由1个带正电荷的质子和1个带正电荷的电子构成 D.由1个带负电荷的质子和1个带负电荷的电子构成 【解析】阅读和理解题意是解答本题的关键。所谓的反粒子就是与正常原子结构中的各种粒子电性相反。结合我们知道的质子是带正电荷,电子是带负电荷的知识,就可得出反氢原子是由1个带负电荷的质子和1个带正电荷的电子构成。 【答案】B 【例题2】(2004·广东省)如下图所示是乙醇分子的模型,则下列说法正确的是( ) 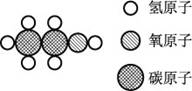 A.该物质是氧化物 B.该物质的化学式是 C.该物质含有四个碳原子 D.大量饮用该物质对人体有益 【解析】从分子的结构图中可观察到分子的构成,从而可得出其化学式为 【答案】B 【例题3】(2005·江苏省海门市)我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律。下表列出的是1~18号元素的部分最高正化合价和最低负化合价。请你阅读后,回答下列问题: 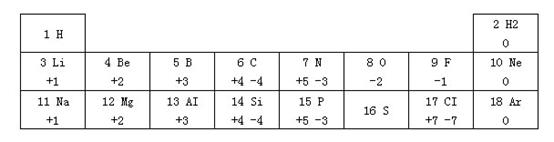 (1)11号元素属于___________元素(填“金属”或“非金属”),它在化学反应中形成的粒子与____________(写元素符号)原子具有相同的核外电子排布; (2)16号元素的原子核外电子数为_________,推测该元素最低负化合价为__________,最高正化合价的氧化物的化学式为_________________; (3)从化合价角度分析,我们可以发现一些规律。请写出其中的一个:___________________。 【解析】(1)11号元素是钠元素,从元素名称的偏旁可知为金属元素。钠原子核外有11个电子,在化学反应中,容易失去最外层电子而转变为只有10个电子的钠离子,而氖元素为10号元素,它的原子核外电子数也是10个,钠离子和氖原子的核外电子排布相同。 (2)原子序数=原子核外电子数,16号元素的原子核外电子数为16。从表中最高正化合价和最低负化合价的递变规律,可推测16号元素的化合价在P(+5、-3)和Cl(+7、-1)之间,即最高正化合价为+6、最低负化合价为-2。 (3)可通过横向、纵向比较元素的最高正化合价和最低负化合价找出有关规律。 【答案】(1)金属Ne(2)16-2+6SO<sub>3</sub>(3)一般地,同一纵行的元素有相同的最高正化合价和相同的最低负化合价;或从左到右,同一横行元素的最高正化合价逐渐升高(+1→+7),最低负化合价也逐渐升高(-4→-1)(或其他合理答案) (责任编辑:admin) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
- 上一篇:第二单元 我们周围的空气 中考试题例析
- 下一篇:自然界的水 知识拓展运用