|
湖北省通山县2008~2009学年度第一学期九年级化学期末考试试题 温馨提示:本次考试内容为人教版九年级化学上册内容。满分为100分。 祝取得好成绩! 可能用到的相对原子质量:C-12 H-1 O-16 Ca-40 Cl-35.5 一、选择题。(共36分。共计18小题,每小题2分;每小题只有一个正确答案,请将正确答案的字母代号填在题号下面的答题栏内。) 1、在加气站应粘贴的安全标志是 A B C D 2、下列能源不应大力开发的是  A.太阳能 B.风能发电 C.水能发电 D.火力发电 3、下列实验操作错误的是 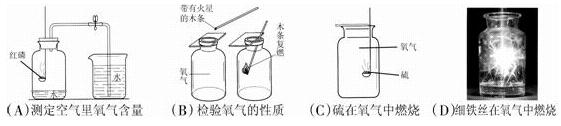 4、富水河是我县最大的河,为了改善水质,防止水被污染,在下面①-④项中,你认为不利于防止水污染的是:①随意丢弃废旧电池到河中 ②生活污水排入河中 ③将生活垃圾倒入河中 ④工业废水经处理后循环使用 A、只有①② B、只有②③ C、只有①④ D、只有①②③ 5、下列变化属于化学变化的是  6、下列日常生活中的物质属于纯净物的是   7、如右图,将两支燃着的蜡烛罩上茶杯,过了一会儿高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从着火燃烧的房间逃离时,下列做法中不正确的是 7、如右图,将两支燃着的蜡烛罩上茶杯,过了一会儿高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从着火燃烧的房间逃离时,下列做法中不正确的是A、用湿毛巾捂住鼻子 B、成站立姿势跑出 C、伏低身子逃出 D、淋湿衣服爬出 8、对下列事实的解释不正确的是
9、“今年过年不收礼,收礼只收脑白金”,脑白金是从深海鱼油中提炼出来的能促进大脑发育的物质,化学式为C26H40O2,关于“脑白金”的叙述错误的是 A.它是由多种元素组成的混合物 B.它的分子中碳、氢、氧原子个数比是13:20:1 C.它是由碳、氢、氧三种元素组成的纯净物  D.它的分子中含有氧原子 D.它的分子中含有氧原子10、在冬天时常常看到煤火炉(如图),炉膛内上层产生蓝色火焰的化 学反应是 A.C+O2  CO2 B.CO2+C CO2 B.CO2+C 2CO 2CO C.2CO+O2  2CO2 D.2C+O2 2CO2 D.2C+O2 2CO 2CO11、1854年法国化学家得维尔,在实验室中意外地发现一种新元素。已知该元素的一个原子中含有40个微粒,其中14个微粒不带电,则该元素是 A.Ca B.N C.Al D.Si  12、某同学利用右图装置测定空气中氧气的含量,红磷燃烧后恢复到室温,打开弹簧夹发现进入广口瓶的液体液面高度超过广口瓶容积的1/5。造成这一现象的原因可能是 12、某同学利用右图装置测定空气中氧气的含量,红磷燃烧后恢复到室温,打开弹簧夹发现进入广口瓶的液体液面高度超过广口瓶容积的1/5。造成这一现象的原因可能是A.实验前没有夹弹簧夹 B.实验装置可能漏气 C.实验中所取的红磷过量 D.实验中所取的红磷不足 13、下列实验现象的描述与相应化学方程式的书写都正确的是 A. 铁丝在空气中剧烈燃烧,火星四射生成黑色固体:3Fe+2O2 B. 水受热至沸腾,产生水蒸气。2H2O  2H2↑+ O2↑ 2H2↑+ O2↑C. 将鸡蛋放入盐酸中,发现鸡蛋表面有气泡产生:CaCO3+2HCl===CaCl2+H2O+CO2↑ D. 烤羊肉串时,看到木炭发红光,放出大量的热:C+O2===CO2 14、下列物质鉴别的方法错误的是 A.区别活性炭和氧化铜——分别投入盛有红棕色二氧化氮的集气瓶中,观察现象 B.区别过氧化氢和蒸馏水——加入MnO2,看是否有气泡 C.区别硬水与软水——常用肥皂水检验,泡沫减少产生浮渣的是硬水 D.区别二氧化碳、氧气和空气——分别将带火星的木条伸入瓶中,观察现象 15、下列物质的用途中,只体现该物质的物理性质的是
A.用二氧化碳灭火 B.氮气作医疗冷冻手术 C.二氧化碳做气肥 D.氧气供动物呼吸 16、下列有关“一定”的说法,正确的是 A、含一种元素的物质一定是单质 B、含有不同元素的纯净物一定是化合物 C、含有两种元素且其中一种为氧元素的物质一定是氧化物 D、含有相同质子数的微粒一定是同种元素  17、如图将插入胶塞的一根光亮的红色铜丝绕成螺旋状,在酒精灯的火焰上烧一段时间后趁热迅速伸入盛有石灰水和X气体的集气瓶中,塞紧胶塞,看到变黑色的铜丝又变为红色,同时石灰水变浑浊,则集气瓶中的气体X是 17、如图将插入胶塞的一根光亮的红色铜丝绕成螺旋状,在酒精灯的火焰上烧一段时间后趁热迅速伸入盛有石灰水和X气体的集气瓶中,塞紧胶塞,看到变黑色的铜丝又变为红色,同时石灰水变浑浊,则集气瓶中的气体X是A.H2 B.O2 C.CO D.CO2  18、“神舟”七号太空行走成功后,大大鼓舞了全国人民的爱国热情,飞船表面的烧蚀材料中含有氮化硅. 己知氮、硅的原子结构示意图依次为(见右图), 则氮化硅的化学式可能是 18、“神舟”七号太空行走成功后,大大鼓舞了全国人民的爱国热情,飞船表面的烧蚀材料中含有氮化硅. 己知氮、硅的原子结构示意图依次为(见右图), 则氮化硅的化学式可能是A、Si3N4 B、Si4N3 C、SiN2 D、SiN 二、填空题。(共40分。除注明外,每空1分) 19、在日常生活中,我们会接触很多化学物质,现在就请你把符合下列要求的化学式填写出来: (1)“干冰”的化学式为_________ (2)目前为止科学家已发现三千多万种物质,若有下列几种元素及化合价 20、为了履行国际社会的《关于消耗臭氧层物质的蒙特利尔议定书》,我国政府决定自2003年6月1日起在全国范围内禁止使用“CTC”作为清洗剂。“CTC”又称四氯化碳,是常用的服装干洗剂,也是修正液(又称涂改液)中的一种溶剂,还是一种优良的灭火剂。根据以上信息回答: (1)“CTC”的化学式为__________,其中碳元素的化合价为_______; (2)推测“CTC”的物理性质是:___________________________。 21、如图是画家用碳墨绘画的我国明朝诗于谦《石灰吟》的国画,诗中写道:“千锤万凿出深山,烈火焚烧若等闲,粉身碎骨浑不怕,要留清白在人间”。试回答:  (1)该字画能够保存多年而不变色,原因是____________________________________。 (2)诗句中“千锤万凿出深山”所体现物质的变化:是__________变化;“烈火焚烧若等闲”所体现的化学反应是石灰石受热分解,该反应是_______反应(填“吸热”或“放热”) (3)“要留清白在人间”指的是石灰水暴露在空气中所发生的化学反应,该化学方程式为__________________________________________(2分)。 22、下图形象的表示甲、乙两物质的变化,其中“●”和“○”分别表示不同的原子 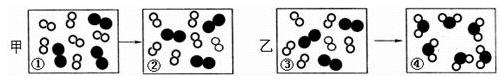 (1)这两个变化的本质区别是:____________________________________________; (2)写出一个符合乙变化的化学方程式_____________________________(2分); (3)四幅图中表示化合物的是______________(填序号). 23、厨房内石油的燃料是液化石油气,主要成分是丙烷,其化学式为C3H8,请你回答下列问题: (1)液化石油气属于化石燃料,目前人类广泛使用的化石燃料有______、_______、______,它们属于 (填“可再生”或“不可再生”)能源。 (2)泄漏的液化石油气能使人窒息,因此安装液化石油气报警器时,应将报警器安在灶台的上方还是下方?理由是(2分) _______________________________________________________; (3)为了检验液化石油气的纯度,当你收集一试管气体后,接下来你的做法是: __________________________________________________(2分); (4)烹饪前要先引燃炉灶,你认为先点火后放气还是先放气后点火,原因是: ___________________________________________________(2分);  当划火柴时,人们发现火焰在上直立火柴,火焰会慢慢熄灭,若慢慢倾斜倒立火柴,则燃烧更旺(如图),原因是(2分): 当划火柴时,人们发现火焰在上直立火柴,火焰会慢慢熄灭,若慢慢倾斜倒立火柴,则燃烧更旺(如图),原因是(2分):________________________________________________________; 液化石油气被点燃后其充分燃烧的化学反应方程式为____________________(2分)。 (5)当炒菜前发现大勺内的油着火,你却没有找到任何盖子去盖上大勺,在不倒掉油的前提下,要想将火熄灭,你的做法是_________________________________(2分),这种灭火的原理是: __________________________________________________________; (6)用餐后洗刷碗碟,判定碗碟是否洗干净的标准是______________________________。 24、汽车工业的发展给人们出行带来了快捷和方便.我县汽车数量近年也迅速增加,在有限的路面上形成“车水马龙”的场面,汽车尾部“吞云吐雾”喷发出大量气体(如图). 据此,你认为汽车增加给人们带来的负面影响是(答二点): ________________________、__________________________; 汽车排放出的有害污染物主要成分是(答二种)______________、______________; 怎样减少汽车尾气对空气的污染,请你提出三点建议: ①_________________________________; ②_________________________________; ③_________________________________。 三、实验探究(共19分。除注明外,每空1分) 25、实验室有下列仪器和高锰酸钾、氯酸钾、石灰石、二氧化锰、稀盐酸五种药品及木块、火柴等实验用品。某同学想利用这些仪器和药品制取某种常见的气体,请回答下列问题: 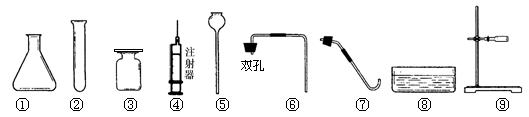 (1)用氯酸钾法制取气体时,缺少的仪器是______,用高锰酸钾制取气体时不仅缺少上述提到的仪器,还缺少用品________,没有这种用品会引起的后果是_________________; (2)利用上述仪器和药品制取大量的某种常见气体,在制取时并能控制反应的速率,选用的仪器是__________________(填标号)。(2分)  26、右图是教材中有关《质量守恒定律》的实验,试回答下列问题: 26、右图是教材中有关《质量守恒定律》的实验,试回答下列问题:(1)反应中观察到的现象是 ________________________________________________ ; (2)左盘锥形瓶口在白磷点燃后要塞紧瓶塞,原因是 ; (3)在实验设计上,玻璃管上方系一瘪气球的目的是 ________________________________________________________________________; 。  27、在研究酸雨的危害时,进行如下探究: 27、在研究酸雨的危害时,进行如下探究:[提出问题]酸雨能腐蚀自然界中的哪些物品呢? [设计实验]实验1:如图,硫在氧气中燃烧,观察到的现象是 ______________________________,实验中出现的错误是__________________________。 若按正确操作,反应后向瓶中倒入蒸馏水,振荡,使SO2与水反应生成亚硫酸H2SO3,一段时间后,亚硫酸与氧气反应生成硫酸,有关方程式为:_________________________、 。 实验2:将所得硫酸型酸雨溶液分成三等分,分别向其中加入如下物质,并观察到如下现象:
 [反思与交流](1)酸雨不仅能腐蚀大理石雕像(如图),还能腐蚀_________________________,有同学提出制取CO2时,不能用大理石和稀硫酸反应,为什么硫酸型酸雨能腐蚀大理石雕像呢?你认为原因是________ [反思与交流](1)酸雨不仅能腐蚀大理石雕像(如图),还能腐蚀_________________________,有同学提出制取CO2时,不能用大理石和稀硫酸反应,为什么硫酸型酸雨能腐蚀大理石雕像呢?你认为原因是__________________________________________。 (2)土壤中有许多细小的石子,有人说酸雨还能加剧“温室效应”,这种说法的依据是: ___________________________________________。 [拓展与应用]怎样防治酸雨产生,请你提出两点建议: ①____________________________; ②_____________________________。 四、计算题(共5分) 28、课外小组的同学研究的课题是测定贝壳中碳酸钙的质量分数,他们取25g贝壳粉碎后放入烧杯中,向杯中倒入稀盐酸,当倒入100g稀盐酸后发现不再产生气泡,并测得烧杯内固体和液体总质量为120.6g (杂质不反应)。求贝壳中碳酸钙的质量分数。 参考答案 一、选择题
二、填空题 19、(1)CO2 (2)①O2 或H2 ②H2O或MgO或K2O 20、(1)CCl4 +4 (2)无色液体易挥发 21、(1)碳的化学性质不活泼 (2)物理、 吸热 (3)CO2+Ca(OH)2===CaCO3↓+H2O 22、(1)甲(前者)是物理变化(或没有生成新物质);乙(后者)是化学变化(有新物质生成)。 (2)2H2+O2  2H2O (3)④ 2H2O (3)④23、(1)煤、石油、天然气 不可再生 (2)装在下方;(经计算)丙烷的密度比空气的密度大。 (3)用拇指堵住集满液化石油气的试管口,管口向上正着移近火焰,移开拇指点火。 (4)先点火后放气,若先放气后点火可能会引起爆鸣或爆炸;火柴燃烧放出热量,使周围的气体受热,密度小于空气,热气体向上运动,木杆直立时没有在热气体中,温度低没有达到着火点(1分)。C3H8+5O2  4H2O+3CO2 4H2O+3CO2(5)把菜放入大勺中;菜吸收了油的热量,使油的温度降到着火点以下。 (6)碗碟上的水既不聚成水滴也不成股流下 24、交通拥挤,噪声污染,空气污染;一氧化碳、氮的氧化物、碳氢化合物、铅的化合物、烟尘(按照教材答出5种污染物中的任意2种污染物即可);①改变汽车发动机中燃油的燃烧方式,②在排气管后安装尾气转化器,③燃烧轻质燃油,如:乙醇汽油。(答案顺序不限) 三、实验探究 25、(1)酒精灯;棉花;高锰酸钾粉末进入导管。 (2)①③④⑥ 26、(1)白磷燃烧,产生大量白烟,发光(或答发出黄色火焰)放热,开始气球胀大冷却后缩小。 (2)防止瓶内气体与空气交换(或防止瓶中的气体逸出,冷却后空气进入瓶中) (3)燃烧时瓶内气体受热膨胀,压强增大,防止塞子被弹起(或为了减压,防止塞子被弹起); (4)1/5: 白磷燃烧最多消耗瓶内氧气,生成固体,使瓶内压强小于外部压强。 27、发出明亮的蓝紫色火焰,产生刺激性气味的气体,放出热量;没有盖玻璃片; SO2+H2O=H2SO3 2H2SO3+O2===2H2SO4 (1)森林和植被(树木)及建筑物(桥梁和楼房);生成的硫酸钙受雨水冲刷,脱离大理石表面,使反应持续进行;(2)酸雨和小石子反应生成二氧化碳,使空气中的二氧化碳增多;①煤进行脱硫燃烧 ②工厂的废气处理后排放 ③开发新型能源(答出两点即给分) 28、解:根据质量守恒定律,生成二氧化碳的质量为 25 g+100 g-120.6 g=4.4 g 设生成4.4 g二氧化碳需碳酸钙质量为x CaCO3+2HCl====CaCl2+H2O+CO2↑(2分) 100 44 x 4.4 g 解得:x=10 g 贝壳中碳酸钙质量分数为: 答:贝壳中碳酸钙的质量分数为40%。 (责任编辑:admin) |

