|
走进《我们周围的空气》 湖北省鄂州市教研室 杨国安 恭喜你,你和你的同学被选为化学科考队的成员。你们的任务是要学习和研究《我们周围的空气》。你们将对“空气的成分”、“空气中氧气含量的测定”、“保护空气”、“氧气的性质”和“实验室制取氧气”等课题进行探究。你们可要努力哟! 空气的成分 科学探究的第一站是“空气的成分”。要求你们了解空气的成分。 空气是由多种成分组成的“大家族”,我们每时每刻都生活在空气的“海洋”里。 空气的成分按体积计算,大约是:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。 需要注意的是,这是按体积计算出来的,不是按质量计算出来的。 了解了空气的成分后,你们就可以开始下面的探究之旅了。 例1 汽车安全气囊内的物质能在碰撞后数秒内迅速反应,生成一种空气中含量最多的气体,该气体是( ) A.氧气 B.二氧化碳 C.氮气 D.稀有气体 答案 C 空气中氧气含量的测定 科学探究的第二站是“空气中氧气含量的测定”。要求你们能解释“探究空气成分”实验的原理和现象,初步了解科学探究的一般过程。  测定原理是:红磷在密闭容器中与氧气反应生成五氧化二磷固体,使容器内压强减小,由于外界大气压强大于容器中气体的压强,水就会被“压”进容器里。通过测定进入容器里水的体积来测定氧气在空气中的体积分数。 测定原理是:红磷在密闭容器中与氧气反应生成五氧化二磷固体,使容器内压强减小,由于外界大气压强大于容器中气体的压强,水就会被“压”进容器里。通过测定进入容器里水的体积来测定氧气在空气中的体积分数。测定装置如右图所示。 要确保实验成功,你还需注意: ⑴红磷要过量,过量的目的是让容器中的氧气完全被消耗。 ⑵装置的气密性要良好。 ⑶待装置冷却到测定前的温度后再读取数据。 上面的内容你已了然于胸了,例2等待着你去探究。 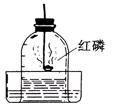 例2 如图是测定空气中氧气含量的实验装置,请回答下列问题: 例2 如图是测定空气中氧气含量的实验装置,请回答下列问题:⑴盛放在燃烧匙中的红磷燃烧时的现象是 。 ⑵在实验中,钟罩内水面所起的变化是 。 ⑶从实验可得出的结论是 ,还可推论出氮气 (填“易”或“难”)溶于水,且其化学性质 (填“活泼”或“不活泼”)。 答案 ⑴发出黄光,产生大量的白烟,放出热量 ⑵水面上升到钟罩内容积的1/5处 ⑶氧气约占空气体积的1/5 难 不活泼 保护空气 科学探究的第三站是保护空气。要求你们增强防治大气污染的环保意识。 人类需要洁净的空气。可工厂烟囱排放出的烟尘,汽车、火车、轮船、飞机喷发出的有害气体,居民炉灶排放出的油烟等,人为地造成了空气污染,严重影响了空气的质量。 空气中的主要污染物有二氧化硫、氮氧化物、一氧化碳以及可吸入颗粒等。对空气质量影响较大的污染物主要来源于化石燃料(煤、石油、天然气)的燃烧和工业排放的废气。 下表列出了几种空气污染物的主要来源:
如何防治大气污染呢?防治大气污染的方法主要是减少排放。 如减少化石燃料的使用;使用清洁能源;研究和使用化石燃料的脱硫技术;改进燃烧装置提高燃烧效率和降低有害气体的排放量;将机动车辆安装尾气净化装置;植树造林,绿化环境等。 了解了空气的污染及其防治后,下面的问题你能解决吗?  例3 随着工业和交通运输业的迅速发展,有害气体和烟尘的排放,对空气造成了严重的污染,控制大气污染的主要途径是减少排放。 例3 随着工业和交通运输业的迅速发展,有害气体和烟尘的排放,对空气造成了严重的污染,控制大气污染的主要途径是减少排放。⑴曾经有过一段时间,许多工厂试图通过建造很高的烟囱来解决排放问题,然而这种做法并没有达到目的,原因是_______________________。如今,通过在烟囱中安装过滤装置,可以有效地控制________的排放;安装烟囱净化洗涤装置,可以除去废气中部分有害气体,根据该装置的净化原理分析,被除去的有害气体所具有的共同性质是______________________。 ⑵按规定汽车应安装尾气处理装置。如在排气管上安装催化转化装置,使尾气中的一氧化碳与一氧化氮在催化剂的作用下,转化为二氧化碳和氮气。该反应的文字表达式为____________________________。 ⑶在控制大气污染方面,你认为还有哪些措施或途径,请写出其中的一种:____________________________。 答案 ⑴污染物的总量并没有减少 烟尘 能溶于水或与水反应 ⑵一氧化碳+一氧化氮 氧气的性质 科学探究的第四站是氧气的性质。要求你们认识氧气的主要性质。 提到氧气,人们首先想到的是地球上的生物体的呼吸离不开氧气,除此之外,氧气还有哪些重要的性质需要你们认识呢? 氧气是无色、无味的气体,密度比空气略大,不易溶于水。这是氧气的物理性质。 氧气的化学性质比较活泼,具有氧化性,是一种常用的氧化剂。 下表是氧气与木炭、硫、红磷、细铁丝反应的具体情况。
相信这些内容你们都掌握了,来解决下列问题吧。 例4 甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原 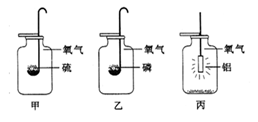 理,进行总结归纳并回答下列问题: 理,进行总结归纳并回答下列问题:⑴所发生的三个反应有多个共同的特点,分别是:①__________;②________;③_______;④_________。(只答四点即可) ⑵甲实验进行时,燃烧匙中硫的状态是_______________。 ⑶任选上述三个实验中的一个,写出反应的文字表达式:________________。 答案 ⑴①都是化合反应;②都是氧化反应;③反应条件都是“点燃”;④都放出热量等等 ⑵液态 ⑶硫+氧气 实验室制取氧气 科学探究的最后一站是实验室制取氧气。要求你们了解制取氧气的主要方法和原理,初步掌握制取氧气的实验技能。 实验室制取氧气的原理是分解过氧化氢溶液、加热氯酸钾或高锰酸钾的方法制氧气。  用高锰酸钾制氧气的装置如右图所示。 用高锰酸钾制氧气的装置如右图所示。一般用排水法收集氧气,因为氧气不易溶于水。 实验室用高锰酸钾制取氧气时,要注意以下几点: ⑴试管口要稍向下倾斜,防止加热时药品里的水分变成水蒸气,到管口冷凝成水珠倒流到试管底部,使试管炸裂。 ⑵高锰酸钾要平铺在试管底部,这样可增大反应物的受热面积,加快反应速率。 ⑶试管口应塞一团棉花,防止加热时高锰酸钾粉末进入导管。 ⑷伸进试管内的导管不宜过长。伸进试管内的导管越长,气体就越难排出。 ⑸加热时,先把试管均匀预热,然后在有药品的地方,稍前部位渐往稍后部位加热,使高锰酸钾有控制的分解,氧气平稳地放出。 ⑹开始加热时排出的是空气,当气泡连续地且比较均匀地放出时,才是氧气,此时才能收集。 ⑺实验完毕后,先将导管移出水面,然后熄灭酒精灯,防止水被倒吸至灼热的试管里,使试管炸裂。 想必以上内容你已很熟悉了,例5将为你本次探究之旅画上圆满的句号。 例5  下图是某同学设计的实验室用加热高锰酸钾制取氧气的装置图。请回答下列问题。 下图是某同学设计的实验室用加热高锰酸钾制取氧气的装置图。请回答下列问题。⑴指出标号仪器的名称:a ;b ;c ;d 。 ⑵简要指出图中的错误并加以改正。 ⑶实验完毕后,应先移去酒精灯还是先把导管从水中拿出来,为什么? 答案 ⑴a—酒精灯;b-试管;c-集气瓶; d-水槽 ⑵①试管口向上倾斜;试管口略向下倾斜。②伸进试管内的导管过长;伸进试管内的导管稍露出胶塞。③试管口处没有放一团棉花;在试管口处放一团棉花 ⑶先把导管从水中拿出,然后熄灭酒精灯。如先熄灭酒精灯,试管内的温度降低,气压下降,水槽中的水就会被倒吸到热的试管中,使试管炸裂 在你们解决了这个问题以后,你们的快乐探究之旅也就要告一段落了。欢迎你们继续探究《滴定·化学》中的其他文章,通过研读这些文章,你们一定会取得丰硕成果的! (责任编辑:admin) |
|||||||||||||||||||||||||||||||||||||||
