2013年中考化学试题汇编——金属和金属材料(五)
http://www.newdu.com 2025/12/21 11:12:39 人民教育出版社 佚名 参加讨论
2013年中考化学试题汇编——金属和金属材料(五) 山东省微山县鲁桥一中 黄尊英 81.(2013.呼和浩特)金属与我们的生活息息相关,在各个领域中用途广泛。 (1)我国第四套人民币硬币从1999年开始发行,一元为钢芯镀镍(Ni),五角币为钢芯镀铜合金,一角币为铝合金或不锈钢。选择铸造硬币的材料不需要考虑的因素是 (填序号)。 A.金属的硬度 B.金属的导电性 C.金属的耐腐蚀性 D.金属价格与硬币面值的吻合度 (2)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残存很少。这说明金、铜、铁这三种金属的活动性由强到弱的顺序是 。 (3)高铁酸钠(Na2FeO4)是一种“绿色环保高效”消毒剂。高铁酸钠中铁元素的化合价为 价。 (4)在质量相等、溶质质量分数相同的稀硫酸中,分别加入等质量的锌粉和铁粉,生成氢气质量(m)随反应时间(t)的变化曲线如下图所示。下列表述正确的是 (填序号)。 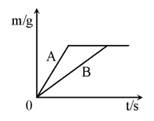 ①A表示锌和稀硫酸的反应曲线 ②反应结束后消耗两种金属的质量相等 ③反应结束后稀硫酸都没有剩余 ④反应结束后两种金属一定都有剩余 ⑤反应结束后生成的氢气质量相等 82.(2013.青岛市)我市某化工厂排放的废液中含有硫酸铜和硫酸亚铁。某化学兴趣小组的同学取了适量的上述废液样品,将一定量锌粉加入样品中,充分反应后过滤,得到滤液A和固体B。 请回答下列有关问题: (1)关于滤液A所含溶质的猜想中,不合理的是 (填写序号)。 ①猜想一:只有硫酸锌 ②猜想二:硫酸锌、硫酸亚铁 ③猜想三:硫酸锌、硫酸亚铁、硫酸铜 ④猜想四:硫酸锌、硫酸铜 (2)设计简单实验,确定“猜想二”对应的固体B的成分: 。 (3)反应后析出金属的质量 (选填“一定”或“不一定”)比参加反应的金属质量小。 83.(2013.泰安市)(3分)下图是初中化学一些常见物质之间转化的关系图(有些反应条件已省略)。其中,A、B、X、Y均为无色气体,E、F为常见金属。已知高温下CO能与多种金属氧化物反应生成相应金属和CO2。请安要求回答下列问题: 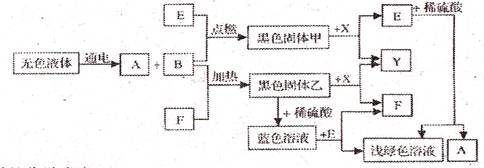 (1)B物质的化学式为 ; (2)蓝色溶液与E反应的化学方程式为 ; (3)黑色固体甲与X反应的化学方程式为 。 84.(2013.安徽省)(6分)铁锅、铝锅是生活中常用的炊具,下图是铁锅的示意图。  (1)铁锅含有合金单质_______(写化学式),含有的有机合成材料是_________。 (2)炒菜时铁锅中的油着火可用锅盖盖灭,其原理是_____________________________。 (3)铝锅轻便、耐用,其原因是__________________、_____________________________。 (4)废旧铁锅、铝锅不要随意丢弃,应回收利用,这样做的意义是_________________。 85.(2013.烟台市)金属材料在我国国防建设中起着重要的作用,因为歼-15飞机在辽宁舰上起飞。  (1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 、 。 (2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果。工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 。 (3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如下图所示的两个实验: 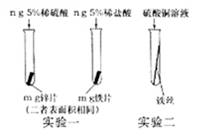 ① 实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是 。 ② 实验二中,若出现 现象,可证明铁的活动性强于铜,该反应的化学方程式为 。 (4)辽宁舰的建造耗费了大量的钢材。某兴趣小组在实验室中用下图所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称量赤铁矿样品的质量为wg)。 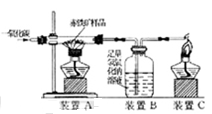 ①装置A中生成铁的化学方程式为 , 装置B中发生反应的化学方程式为 。 ②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是 或 。 86.(2013.安徽省)“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。 【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢? 【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。 【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
(1)写出稀硫酸与锌反应的化学方程式________________________________________。 (2)小兵用下图装置收集并测量氢气的体积,其中量筒的作用是___________________,氢气应从________(填e或f或g)管通入。 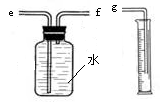 【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。 【得出结论】(4)结论______________________________________________。 【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分) (5)下表是小兵第①组实验的详细数据。
请描述锌与硫酸反应的快慢的变化并解释原因__________________________________。 (6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。_________________________。 87.(2013.襄阳市)化学材料的发展和应用,推动了社会的进步。铁、铜、铝、棉花、聚乙烯塑料等都是人们生活和生产中常见的材料。 (1)上述材料中,属于天然有机高分子的是 ; (2)铝表面易形成一层致密的保护膜,其成分是 ; (3)为了防止水龙头生锈,其表面常镀一层铬,其防锈的原理是: 。 参考答案: 81.(1)B (2)铁>铜>金(或Fe>Cu>Au)(3)+6 (4)①③⑤ 82.(1)④ (2)取一定量固体B于试管中,加入适量的稀盐酸,若无气泡产生,则固体B是铜,若用气泡产生,则固体B的成分是铜和铁 (3)一定 83.(1)O2 (2)CuSO4 + Fe === FeSO4 + Cu (3)4CO + Fe3O4 84.(1)Fe;塑料。(2)使油与氧气隔绝。 (3)铝的密度小、常温下,与氧气反应表面生成致密的氧化铝薄膜,阻止铝的进一步氧化。 (4)减少环境污染,节约金属资源。 85.(1)强度大 质量轻(或硬度大,耐腐蚀等合理答案均可) (2)氧气、水蒸气 Fe2O 3 + 6HCl =2FeCl3 + 3H2O (3)选取酸的种类不同 铁丝表面有红色的物质 Fe + CuSO4 === FeSO4 + Cu (4)3CO+ Fe2O3 反应前后装置A减少的质量(或反应后装置A中药品的质量)反应前后装置B增加的质量(或反应前后装置B中药品增加的质量) 86.(1)Zn+H2SO4=ZnSO4+H2↑。 (2)根据进入量筒中水的体积,判断生成氢气的体积;F。 (3)①③或②④。 (4)硫酸的质量分数越大,反应速率越快/锌与硫酸的接触面积越大,反应速率越快。 (5)由慢到快然后逐渐减慢;随着反应的进行,硫酸被消耗,硫酸溶质质量分数变小。 (6)温度;取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间。(只要考生有控制变量的意识即可) 87.(1)棉花 (2)氧化铝 (3)隔绝水和空气 (责任编辑:admin) |
- 上一篇:《盐 化肥》单元测试B
- 下一篇:第九单元 溶液 综合检测