2013年中考化学试题汇编——金属和金属材料(六)
http://www.newdu.com 2025/11/06 02:11:22 人民教育出版社 佚名 参加讨论
2013年中考化学试题汇编——金属和金属材料(六) 山东省微山县鲁桥一中 黄尊英 88.(2013.莱芜市)人类生活生产离不开金属,不仅因为其物理性能优良,还与化学性质密切相关。 (1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高。钛和钛合金是新型的结构材料,主要用于航天和航海工业。上述描述中属于钛化学性质的是 。 (2)某小组用图所示装置对铁生锈的条件进行探究。4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是 。  (3)工业生产常用10%的稀盐酸来除铁锈,写出除锈的化学方程式 。 实验室用浓盐酸配制10%稀盐酸时,用到的主要仪器有 。 (4)在金属活动顺序表中,金属位置越靠前,越容易失去电子。Ca、 Mg、 K三种金属失电子能力由强到弱的顺序是 ,如图是三种原子的结构示意图,据此推测金属失电子能力的强弱除与最外层电子数有关外,还可能与 有关。 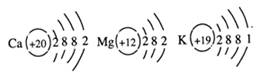 89.(2013.安徽省)(7分)以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如下: 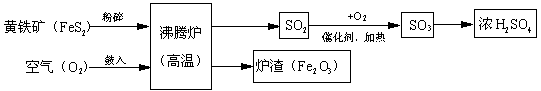 (1)写出流程图中一种氧化物的名称___________。 (2)将黄铁矿粉碎,目的是_______________________________________________。 (3)流程中SO2转化为SO3的化学方程式为_________________________________。 (4)实验室稀释浓硫酸应注意什么?__________________________________。 (5)炉渣(Fe2O3)在工业上可用来_____________________________________________。 90.(2013.荆门市)用金属铁制备自来水的新型消毒、净水剂K2FeO4的流程如下: 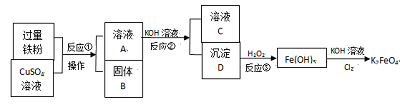 请回答下列问题: ⑵ 体B的成分是 (用符号表示); ⑵操作I的名称是 ; 操作I所需要的仪器和用品:铁架台、玻璃仪器、试剂、 (填一种实验物品名称)。 ⑶反应①、②、③中没有涉及到的化学反应类型是 (填字母代号) A.化合反应 B.分解反应 C.置换反应 D.复分解反应 ⑷请书写下列反应的化学方程式: 反应② ; 反应③ 。91.(2013.内江市)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是 。 ①Fe、Ag、CuSO4溶液 ②Cu、Ag、FeSO4溶液 ③Cu、FeSO4溶液、AgNO3溶液 在你认为可行的试剂组中,写出其中发生反应的化学方程式 (若可行的试剂不只一组,请任选其中一组)。 92.(2013年德阳市)金属钛(Ti)的合金具有耐高温、耐腐蚀、强度高等性能,所以,钛合金广泛用于航空、航天工业及化学工业。工业上冶炼金属钛的过程是以钛矿石(主要成分为钛酸亚铁,化学式为FeTiO3)、焦炭、氯气为原料,在高温条件下制取TiCl4,其反应的化学方程式为:2FeTiO3 + 6C + 7Cl2 请根据以上信息回答下列问题: (1)FeTiO3中钛元素的化合价为 。 (2)在制备TiCl4的反应中,X的化学式为 。 (3)镁与TiCl4反应的化学方程式为 。 93.(2013?东营)人类的生产生活离不开金属材料. (1)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属 的位置移到最后,正好符合由弱到强的 顺序. (2)铝、铁、铜  (3)铜也容易生锈,铜锈的主要成分是碱式碳酸铜(Cu2(OH)2CO3),是铜与空气中的氧气、水和 共同作用的结果. (4)合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据.
①铅铅锡合金中某种金属的质量分数与合金的熔点有如图2所示的关系,其中横坐标表示的是 的质量分数;当合金熔点最低时,合金中铅与锡的质量比为 . ②保险丝由铋、铅、锡、镉组成,其熔点约为 .[来源:学。科。网] A.15~30℃; B.60~80℃; C.235~250℃; D.300~320℃. 94.(2013?聊城)下水道堵塞是日常生活中经常遇到的问题.“管道通”可使堵塞的管道畅通无阻.某同学对此很好奇,于是想探究“管道通”中物质的成分.请与该同学一起探究: 【提出问题】“管道通”中的物质是什么? 【查阅资料】 (1)下水管里的淤积物主要为油污、食物残渣、毛发等. (2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道. (3)铝粉呈银灰色.铝与酸、强碱溶液都能反应放出氢气,同时放出 ①铝与盐酸反应的化学方程式是 . ②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+ ═2NaAlO2+3H2↑ 【猜想与验证】打开一盒管道通,内有一袋白色固体颗粒和一袋银灰色粉末. (1)猜想:白色固体颗粒为氢氧化钠.
结论:白色固体颗粒为氢氧化钠. (2)猜想:银灰色粉末为铝粉. 实验:取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中 滴加 溶液,都产生大量气泡且试管外壁温度明显升高,点燃反应产生的气体火焰均呈淡蓝色. 结论:银灰色粉末为铝粉. 【应用】使用“管道通”时,先将银灰色粉状固体添加入 A.管道内温度明显升高 B.产生大量气体 C.反应放出大量热 D.气体燃烧后,火焰成淡蓝色. 参考答案: 88.(1)能与N2反应(2)O2的浓度(或O2的量) (3)Fe2O3 + 6HCl =2FeCl3 + 3H2O 量筒、烧杯、玻璃棒 (4)K、Ca、Mg 电子数 89.(1)二氧化硫或三氧化硫或三氧化二铁。 (2)增大反应物的接触面积。 (3) (4)将浓硫酸没器壁慢慢倒入水中,边倒边搅拌,且不可将水倒入浓硫酸中。 (5)做治铁原料。 90.(1)、Cu、Fe (2)、过滤、滤纸 (3)、B (4)、 91.② Fe+CuSO4 = FeSO4+Cu Cu+2AgNO3 = Cu(NO3)2+2Ag 92.(1)+4 (2)FeCl3 (3)TiCl4 + 2Mg 93.(1) 铁 金属活动性 (2) A BC (3) 二氧化碳 (4) ①锡 2:3 ② B 94.【查阅资料】①2Al+6HCl═2AlCl3+3H2↑ ②2H2O 【猜想与验证】(1)试管外壁发烫 (2)氢氧化钠 【应用】 ABCD (责任编辑:admin) |
- 上一篇:第九单元 溶液 综合评估
- 下一篇:《盐 化肥》单元测试A