《酸和碱》单元测试B
http://www.newdu.com 2025/11/06 12:11:32 人民教育出版社 佚名 参加讨论
《酸和碱》单元测试B 天津市滨海新区塘沽第二中学 张 辉 天津市滨海新区塘沽第二中学 张 怡 一、选择题 1.柠檬汁能使紫色石蕊溶液变成红色,由此可知,柠檬汁( )。 A.显碱性 B.显酸性 C.显中性 D.无法确定 考查目的:石蕊的变色规律。 答案:B。 解析:应用紫色石蕊溶液遇酸变红、遇碱变蓝的变色规律,即可得出答案。 2.为了检验一桶实验室用的蒸馏水是否被某种酸污染,下列几种做法可取的是( )。 A.取样品,用嘴品尝 B.观察颜色 C.取样品,向其中滴入酚酞溶液 D.取样品,向其中滴入石蕊溶液 考查目的:酸的检验。 答案:D。 解析:A:违反药品取用原则;B、C:无论蒸馏水是否被酸污染,均没有明显现象,所以不可取;D:若石蕊变红,则被酸污染。 3.下列物质长期放置在空气中,溶液质量和溶质质量都会减少的是( )。 A.食盐溶液 B.浓硫酸 C.浓盐酸 D.蔗糖溶液 考查目的:常见酸、碱、盐的特性。 答案:C。 解析:浓硫酸具有吸水性,因此溶液质量会增大,溶质质量不变。浓盐酸具有挥发性,能挥发出氯化氢气体,因此溶液质量会减小,溶质质量也减小。食盐溶液、蔗糖溶液长期放置在空气中,由于水分挥发,溶液质量减少,溶质质量不变。 4.小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适的物质对铁锈进行处理,这种物质是( )。 A.汽油 B.食盐水 C.白醋 D.米酒 考查目的:酸的用途。 答案:C。 解析:白醋中含有醋酸,铁锈能与醋酸反应。 5.用一种试剂就能把石灰水、稀盐酸和食盐水三种溶液区别开,这种试剂是( )。 A.酚酞溶液 B.紫色石蕊溶液 C.水 D.酒精 考查目的:酸、碱的化学性质。 答案:B。 解析:能使石蕊变红的原溶液是盐酸,能使石蕊变蓝的原溶液是石灰水,不能使石蕊变色的原溶液是氯化钠溶液。 6.(2013年天津改编)下列事实与相应的解释不一致的是( )。
考查目的:分子、常见的碱、氮气的性质。 答案:A。 解析:A中混合后体积变小的原因是分子之间有间隔,所以A选项事实与解释不一致;B中不同的碱具有相似化学性质的原因是溶液中都含有氢氧根离子,所以B选项事实与解释一致;C中氮气的化学性质不活泼,可用作焊接金属时的保护气,所以C选项事实与解释一致;D中溶液导电的实质是溶液中存在着可自由移动的离子,所以D选项的解释和事实一致。 7.据报道,某地一辆运输浓盐酸的车辆发生事故,导致酸液泄漏闹市,经喷水和撒石灰处理后,排除了险情。对喷水和撒石灰作法的叙述错误的是( )。 A.喷水可以减少浓盐酸挥发 B.喷水可以降低盐酸的酸性 C.撒石灰为了消除盐酸污染 D.喷水是尽快把盐酸冲进下水道 考查目的:盐酸的性质。 答案:D。 解析:泄漏的酸性物质应该用碱液中和,降低酸对环境的危害。喷水是为了稀释酸,降低盐酸的酸性。 8.将滴有酚酞溶液的蒸馏水注入U形管中,然后向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。下列说法正确的是( )。 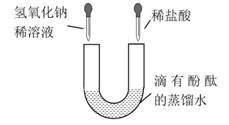 A.开始时左边溶液呈蓝色,右边溶液呈红色 B.开始时左边溶液呈无色,右边溶液呈红色 C.充分反应后U形管中溶液一定呈无色 D.充分反应后U形管中溶液可能呈红色 考查目的:考察指示剂遇酸、碱的变色情况,以及酸碱中和的知识。 答案:D。 解析:酚酞遇碱变红,遇酸不变色。初始滴入时,可能存在左侧变红、右侧无色的现象。如果酸和碱恰好完全反应,则充分混合后U形管中的溶液应呈无色。但是本题并未给出酸、碱的浓度,因此,反应后的溶液可能偏酸性,也可能偏碱性,还可能呈中性。 9.许多植物的花汁可以作酸碱指示剂。下表是菊花浸出液在不同条件下的显色情况。在肥皂水(pH:9.5~10.5)中滴加菊花浸出液,溶液显示的颜色是( )。
A.无色 B.红色 C.黄色 D.紫色 考查目的:溶液酸碱性与pH的关系。 答案:C。 解析:肥皂水的pH为9.5~10.5,说明呈碱性。 10.用pH试纸测得家庭常用洗涤剂的pH如下表所示:
在没有除锈剂的情况下,可以用来代替除锈剂的是( )。 A.厕所清洁剂 B.洗发精 C.洗衣液 D.厨房清洁剂 考查目的:结合酸的化学性质和溶液pH的相关知识,解决实际问题。 答案:A。 解析:酸可以和金属氧化物反应,用来作为除锈剂,厕所清洁剂pH为1,显酸性。 二、填空题 1.某化学兴趣小组采用下列花汁制作酸碱指示剂,实验记录如下:
根据以上信息回答: (1)小明用月季花的花汁,检测附近造纸厂排放废水的酸碱性,溶液呈浅红色,则此废水显 性。 (2)小芳用玫瑰花的花汁,检测家中花盆土壤的酸碱性,溶液呈绿色,则此花盆的土壤显 性。 (3)小军已检验出纯碱溶液显碱性,他不可能选择的花汁是 。 考查目的:利用自制指示剂鉴别物质的酸碱性。 答案:(1)酸 (2)碱 (3)万寿菊 解析:从植物的花、叶、果实中提取的汁液,只要在酸、碱溶液中显示不同的颜色,就可用来代替石蕊和酚酞作为酸碱指示剂。从上表可知,红玫瑰、月季花都能与酸或碱作用显示不同的颜色,可用作酸碱指示剂;万寿菊对酸或碱显示同一颜色,不宜用作酸碱指示剂。 2.生锈的铁钉放入足量的稀盐酸中,片刻观察到的现象是 ;发生反应的化学方程式为 ;反应一段时间后,又观察到的现象是 ,发生反应的化学方程式为 。 考查目的:酸与金属氧化物、活泼金属的反应。 答案:铁锈消失,溶液由无色变为黄色 Fe2O3+6HCl=2FeCl3+3H2O 溶液中有无色气泡产生 Fe+2HCl=FeCl2+H2↑ 解析:铁锈的主要成分是氧化铁,它与盐酸反应生成氯化铁和水,因此溶液显黄色。当铁钉表面的铁锈反应完后,露出的铁也会与盐酸反应,生成氯化亚铁和氢气。 3.(2013年青海)敞口放置的浓硫酸、浓盐酸和氢氧化钠,一段时间后其中质量增加且发生化学变化的是 ,该反应的化学方程式是 。 考查目的:浓硫酸、浓盐酸和氢氧化钠的性质,以及物理变化与化学变化的区别。 答案:氢氧化钠 2NaOH+CO2=Na2CO3+H2O 解析:氢氧化钠敞口放置在空气中,不仅能吸收空气中的水分而潮解,而且能与空气中的二氧化碳发生化学反应,生成碳酸钠和水,从而质量增加,故氢氧化钠符合题目要求。浓盐酸具有挥发性,敞口放置在空气中一段时间后,其质量会减少,故浓盐酸不符合题目要求。浓硫酸具有吸水性,敞口放置在空气中一段时间后,会因吸收空气中的水分而使其质量增加,但上述过程属于物理变化,故浓硫酸不符合题目要求。 4. 和 生成 和水的反应,叫做中和反应。中和反应的实质是酸解离出的 与碱解离出的 反应生成水。中和反应是复分解反应中的一种。 考查目的:中和反应的本质。 答案:酸 碱 盐 H+ OH- 解析:略。 5.氢氧化钠(化学式: )因有强烈的腐蚀性,故俗称为 、 或 ,白色固体, 溶于水,且放出大量的热,暴露在空气中容易吸收水分发生潮解;可用于干燥中性或碱性气体(如O2、H2、NH3等),但不能干燥酸性气体(如 、 、 等)。由于在空气里氢氧化钠不仅能吸收水分而潮解,还能与空气里的 起反应而变质。写出有关反应的化学方程式: 。因此氢氧化钠必须 保存。 考查目的:氢氧化钠的性质。 答案:NaOH 火碱 烧碱 苛性钠 易 CO2 SO2 HCl 二氧化碳 2NaOH+CO2=Na2CO3+H2O 密封 解析:略。 (责任编辑:admin) |
- 上一篇:2013年中考化学试题汇编——溶液(一)
- 下一篇:第九单元 溶液 综合评估