北京市崇文区2008—2009学年度第一学期初三化学期末统一练习
http://www.newdu.com 2025/11/08 09:11:32 人民教育出版社 佚名 参加讨论
北京市崇文区2008—2009学年度第一学期初三化学期末统一练习 李菁菁(供稿) 可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5 K-39 Mn-55 Fe-56 Cu-64 Zn-65 Ag-108 第Ⅰ卷(选择题 共25分) 一、选择题(每小题只有1个选项符合题意。共25个小题,每小题1分,共25分。) 1.下列是生活中常见的一些变化,其中属于化学变化的是 A.天热吃雪糕时,发现雪糕慢慢熔化 B.潮湿的衣服在空气中放置会晾干 C.洗净的铁锅常会出现锈迹 D.夏天从冰箱取出的瓶子外壁迅速附着一层水 2.下列元素中,属于金属元素的是 A.氖 B.锌 C.氧 D.磷 3.下图中的符号表示2个氢原子的是 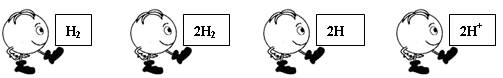 A B C D 4.2008年5月17日,在“5?12汶川大地震”抗震救灾现场,自贡市疾病预防控制中心的防疫人员受到了胡锦涛总书记的接见,当时他们正在喷洒一种“含氯消毒液”。 “含氯消毒液”中的“氯”在这里指的是 A.元素 B.原子 C.分子 D.离子 5. 分子、原子、离子都是构成物质的粒子。下列物质由分子直接构成的是 A. 铜 B. 氧气 C.金刚石 D. 氯化钠 6.以下是四种常用的危险品标志,在装运乙醇的包装箱上应贴的标志是  7.下列物质在氧气中燃烧,生成黑色固体物质的是 A.硫粉 B.木炭 C.白磷 D.铁丝 8.某种冷烫精的主要成分是溴酸钠(NaBrO3),溴酸钠对皮肤有剌激作用,使用不当会引起皮炎。溴酸钠中溴(Br)元素的化合价为 A.+5 B.+4 C.+3 D.+1 9.下列试剂瓶的标签上,化学式书写正确的是 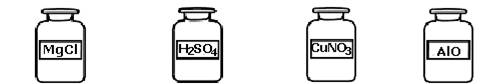 A B C D 10.水是人类生活中不可缺少的物质。下列关于水的说法或做法中正确的是 A.过滤能除去水中所有杂质 B.工业废水若无色澄清就可以直接排入河中 C.地球上的淡水资源储量丰富 D.水的污染会引起土壤污染 11.正确的化学实验操作对实验结果及人身安全都非常重要。下图所示实验操作中,正确的是 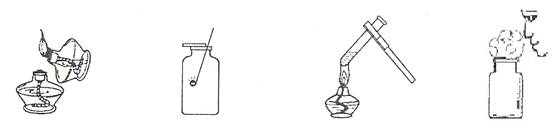 A.点燃酒精灯 B.氧气验满 C.液体加热 D.闻气体气味 12.下列净化水的方法中,净化程度最高的是 A.沉淀 B. 吸附 C.过滤 D.蒸馏 13.下列操作中,可以鉴别空气、氧气和二氧化碳三瓶气体的是 A.倒入石蕊溶液 B.闻气体的气味 C.倒入澄清的石灰水 D.插入燃着的木条 14.下列化学方程式书写正确的是 A.铁丝在氧气中燃烧:4Fe+3O2  2Fe2O3 2Fe2O3B.红磷在氧气中燃烧:2P + 5O2  P2O5 P2O5C.铁和硫酸反应:2Fe+3H2SO4=== Fe2 (SO4)3+3H2↑ D.氢气在氧气中燃烧:2H2 + O2  2H2O 2H2O15.今年4月22日是第39个“世界地球日”,我国确定的主题是“善待地球—从身边小事做起”,下列行动不符合这一主题的是 A.大量植树造林 B.大量使用塑料袋 C.回收废旧电池 D.节约用水 16.下列各原子结构示意图中所表示的原子中,具有相对稳定结构的是  17.下列关于氧气性质的叙述错误的是 A.通常状况下不易溶于水 B.通常状况下密度略大于空气 C.在与其它物质的反应中大多表现出可燃性 D.通常状况下是无色无味气体 18.人类每年从自然界中提取大量的金属铁,下列关于铁的说法正确的是 A.钢是很纯的铁 B.生铁是含少量碳的铁合金 C.被腐蚀的铁制品属于不可回收垃圾 D.炼铁的过程是把金属铁变成氧化铁 19.下列叙述完全符合质量守恒定律的是 A.水结成冰前后,质量保持不变 B.50mL水和50 mL乙醇混合后总体积小于100 mL C.在100 g过氧化氢溶液中,含有30 g过氧化氢和70 g水 D.1.2g碳与3.2 g氧气反应可生成4.4g二氧化碳 20.科学家计划用质子数为20的钙离子,轰击核电荷数为98的锎元素靶,使两元素的原子核合并在一起,合成核电荷数为118的新元素。对此理解正确的是 A.新元素的原子序数为116 B.新元素原子的质子数为118 C.新元素的相对原子质量为118 D.变化过程中元素种类没有发生改变 21.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下: 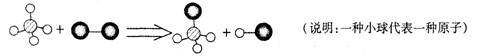 则下列说法正确的是 A.图示中共有4种分子 B.该反应属于化合反应 C.图示中的反应物都是单质 D.该图示不符合质量守恒定律 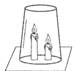 22.如右图,将两支燃着的蜡烛罩上茶杯,过了一会儿,高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从发生火灾的房间逃离时,下列做法中不正确的是 22.如右图,将两支燃着的蜡烛罩上茶杯,过了一会儿,高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从发生火灾的房间逃离时,下列做法中不正确的是A.用湿毛巾捂住鼻子 B.成站立姿势跑出 C.伏低身子逃出 D.淋湿衣服爬出 23.森林初发火灾时,可以使用爆炸灭火的方法,将灭火弹抛到火场使之爆炸并将火扑灭。关于爆炸灭火原因及应用分析不合理的是 A.爆炸使燃烧处于暂时缺氧状态 B.此法能有效解决缺水地区火灾灭火问题 C.爆炸气浪降低了可燃物的着火点 D.爆炸掀起的沙土能覆盖可燃物,隔绝空气 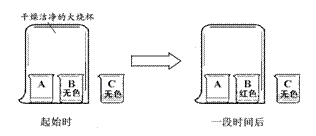 24.A、B、C三只小烧杯内分别依次盛有一定体积的浓氨水、滴有酚酞溶液的蒸馏水、滴有酚酞溶液的蒸馏水,按下图所示进行探究活动,不能得到的结论是 24.A、B、C三只小烧杯内分别依次盛有一定体积的浓氨水、滴有酚酞溶液的蒸馏水、滴有酚酞溶液的蒸馏水,按下图所示进行探究活动,不能得到的结论是A.水能使酚酞溶液变红 B.氨水能使酚酞溶液变红 C.空气不能使酚酞溶液变红 D.浓氨水易挥发,氨气易溶于水 25.已知某物质中含有元素M(注:M代表一种金属元素),其化学式可表示为MSO4,相对原子质量为160。则M的元素符号及MSO4中M元素的质量分数为 A.Fe65% B.Fe35% C.Cu60% D.Cu60% 第II卷(非选择题共55分) 二、填空题(每空1分,共29分。) 26.(6分)分类是学习和研究物质及其变化的一种常用方法,分类要有一定的标准。 (1)请你按照物质组成标准分类的方法,模仿示例,在空格处填上适当的化学式。  (2)下列分别盛有不同物质的容器中,所盛物质属于单质的是_____,属于混合物的是______,属于氧化物的是_______。(均填字母) 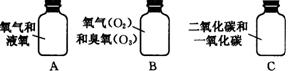   27.(5分)(1)向盛有水的烧杯中加入少量品红,静置一段时间后,溶液逐渐变成红色,此实验主要说明分子的性质是 。将所得溶液通过右图A的简易净水器处理后,可得到无色溶液,由此说明活性炭可以吸附 物质。 27.(5分)(1)向盛有水的烧杯中加入少量品红,静置一段时间后,溶液逐渐变成红色,此实验主要说明分子的性质是 。将所得溶液通过右图A的简易净水器处理后,可得到无色溶液,由此说明活性炭可以吸附 物质。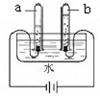 (2)利用右图B装置进行水的电解实验,试管b中收集的气体是 ,反应的化学 (2)利用右图B装置进行水的电解实验,试管b中收集的气体是 ,反应的化学方程式为 ,由此实验说明水是由__________元素组成的。 28.(5分)燃料的使用,给人们的生活带来了很多方便。 (1)煤是目前人类生产、生活中的主要燃料,它燃烧时产生 (填一种气体的名称或化学式)气体,该气体溶于雨水,会形成酸雨危害环境。 (2)我国农村常用沼气来替代化石燃料和柴禾,沼气中的主要成分燃烧的化学方程式为: 。 (3)人类目前所使用的最清洁的燃料是,由于其制取成本高和贮存困难,作为燃料还不能广泛应用。为了普及氢动力汽车,科学家仍在不懈努力。据英国《新科学家》杂志报道,以色列科学家发明了一种车用制氢装置,装置中制氢气的原理为:硼(B)和水在高温下反应,生成氢氧化硼[B(OH)3]和氢气。其反应的化学方程式为________________________________________,该反应属于 反应。 29.(7分)人类的生产生活离不开金属。 (1)在地壳里含量居第二位的金属元素是 。 (2)下列铜制品的用途中,利用金属导电性的是 (填字母)。  A.铜火锅 B.铜导线 C.铜钟 D.铜钱 (3)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝。金属大规模被使用的先后顺序跟_____________(填字母)关系最大。 A.地壳中金属元素的含量 B.金属的导电性 C.金属的活动性 (4)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等浓度的足量稀盐酸中(反应中Mn显+2价),请回答:
除了比较金属与酸反应产生气体速率的快慢,请你再举出一种可比较这二种金属活动性强弱的方法(写出所需药品即可):_____________和___________。 (5)将盛有等质量、等浓度稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断: ①若天平仍保持平衡,烧杯中一定没有剩余的物质是____________; ②若天平失去平衡,则指针一定偏向放_____________的一边。 30.(6分)A、B、C、X、Y均为初中常见的纯净物,它们之间有如下转化关系(部分生成物已略去) 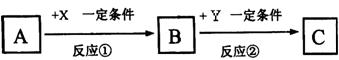 (1)若X、Y为同种物质,且为氧气,A是 (写化学式)。 (2)若A、C为同种物质,则反应①、②的化学方程式为: ① ; ② 。 (3)若A、B、C三种物质的组成中都含有一种相同元素,且X和Y在一定条件下可以发生化学反应,则C的化学式为 ,A与X反应的化学方程式为 。 (4)若A与Y在一定条件可以直接转化为C,且A、B、C均为化合物,B、A、C的相对分子质量依次递增,则A、B、C三种物质的化学式分别为 、 、 (共1分)。 三、实验题(除特殊注明外,每空1分。共19分。) 31.(8分)(1)规范的实验操作是实验成功的前提。请回答: ①量取8mL稀硫酸,应选用__________(填字母)的量筒。 A.5mL B.10mL C.100mL ②往试管里装固体粉末,通常使用_________(填字母)。 A.镊子 B.玻璃棒 C.药匙(或纸槽) (2)请结合下图所示实验装置回答有关问题:  ①写出装置中标号仪器的名称:a____________。 ②写出一个实验室制取氧气的化学方程式____________________________ 。 根据该反应原理,可选择上图中______________(填字母)与___________(填字母)组装一套制取氧气的装置。 ③实验室制取二氧化碳的化学方程式为______________,你所组装的上述制取氧气的装置_______(填“能”或“不能”)用于实验室制取二氧化碳。 32.(5分)如下图A所示,取一个大烧杯,在里面装入约1/2的细沙;烧杯一边的细沙中,插入高低不同的两支蜡烛;将截取瓶底的大口饮料瓶做成简易漏斗,取三张用石蕊溶液染成紫色的干燥小纸条,将一张干燥的和一张润湿后的纸条(润湿后仍为紫色)粘在简易漏斗的内壁,将另一张纸条润湿后,粘在简易漏斗的外壁,将漏斗插入细沙的另一边。按下列各步骤继续实验,并回答有关问题。  图A 图B 图C (1)如图A,用以收集满二氧化碳的集气瓶(集气瓶的容积与简易漏斗内容积相当)向漏斗内慢慢倒入气体,可以观察到的实验现象是 (填字母); A.漏斗内干燥的纸条变成红色,漏斗内、外壁湿润的纸条都不变色 B.漏斗外壁上湿润的纸条变成红色,漏斗内干燥及湿润的纸条都不变色 C.漏斗内壁上湿润的纸条变成红色,漏斗内干燥的纸条和外壁湿润的纸条都不变色 由此现象能够得出的结论是: (2分)。 (2)如图B所示,快速点燃两支蜡烛。 (3)如图C所示,将漏斗向上慢慢提起至下端高于烧杯口,可以观察到的实验现象是: ,根据此现象能够得出的结论是 。 33.(6分)某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究。探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。 【查阅资料】白磷的着火点是40 ℃,红磷的着火点是240 ℃,……燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,并能与空气中的水蒸气反应,生成有毒的偏磷酸(HPO3)。 【变流与讨论】白烟对人体健康有害,该实验装置必须改进。 【改进与实验】同学们按改进后的图2装置进行实验。  图1 图2 图3 请你帮助他们将下表补充完整。
【反思与评价】 (1)改进后的图2装置与图1装置比较的优点是: 。 (2)小林同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是: (填字母)。A.收集生成的气体 B.防止有害物质污染空气 C.调节试管内的气体压强,避免橡皮塞因试管内气体热膨胀而松动 【拓展与迁移】 实验小结时,小朱同学说:“待a试管冷却后,如果将试管口朝下垂直伸入水面下(室温),并取下橡皮塞,将看到液体进入试管。”这一说法得到大家的一致认同。 你认为如果不考虑橡皮塞占试管的容积,且实验所用白磷足量,装置气密性良好,进入a试管内液体的体积约占试管容积的,理由是 。 四、计算题(共7分) 34.(4分)实验室常用锌和稀硫酸反应制氢气。若制取0.2 g氢气,需要锌的质量是多少?  35.(3分)小强的妈妈要焙制面包,叫小强去商店买一包纯碱,小强仔细看了包装说明(如下图),并产生疑问:这包纯碱中Na2CO3的质量分数是否如说明所标注的一样,不小于98%呢? 35.(3分)小强的妈妈要焙制面包,叫小强去商店买一包纯碱,小强仔细看了包装说明(如下图),并产生疑问:这包纯碱中Na2CO3的质量分数是否如说明所标注的一样,不小于98%呢?回到学校,小强取出从家里带来的一小包纯碱样品进行实验:准确称取5.5 g样品放入烧杯中,向其中滴加盐酸至刚好完全反应(忽略CO2溶于水),共用去稀盐酸25 g,得到溶液质量为28.3 g(注:杂质溶于水,且与盐酸不反应。碳酸钠与盐酸反应的化学方程式为:Na2CO3 +2HCl == 2NaCl + H2O + CO2↑)求: (1)生成CO2的质量; (2)通过计算判断纯碱样品中碳酸钠的质量分数是否与包装说明相符。(计算结果精确到0.1%) 参考答案及评分批准 一、选择题(每小题只有一个选项符合题意。共25个小题,每小题1分,共25分。)
二、填空题(共29分,每空1分) 26.(6分)(1)A:N2B:CO2C:CH4 (2)AB、C、ED 27.(5分)(1)分子在不断地运动 有色 (2)O2(或氧气)2H2O  2H2↑ + O2↑氢、氧(或H、O) 2H2↑ + O2↑氢、氧(或H、O)28.(5分)(1)二氧化硫[或SO2、或二氧化氮(NO2)] (2)CH4+ 2O2  CO2+ 2H2O CO2+ 2H2O(3)H2 2B + 6H2O ===== 2B(OH)3 + 3H2↑ 置换 29.(7分)(1)铁(或Fe)(2)B(3)C (4)<金属锰和硫酸亚铁溶液 (5)①盐酸 ②铁 30.(6分)(1)C (2)①CaCO3 + 2HCl == CaCl2+ H2O + CO2↑ ②CO2 + Ca(OH)2 == CaCO3 ↓+ H2O 或:①CO2 + Ca(OH)2 == CaCO3 ↓+ H2O ②CaCO3 + 2HCl == CaCl2+ H2O + CO2↑ (3)Fe3O4 Fe2O3+ 3CO  2Fe + 3CO2 2Fe + 3CO2(4)CuSO4、FeSO4、ZnSO4 注:此题其他合理答案均得分。 三、实验题(共19分。除特殊注明外,每空1分。) 31.(8分)(1)①B ②C (2)①试管② 2H2O2 ③ CaCO3 + 2HCl == CaCl2+ H2O + CO2↑ 注:此题其他合理答案均得分。 32.(5分)(1)C 水和二氧化碳都不能使紫色石蕊变成红色,二氧化碳与水反应的生成物(碳酸)能使紫色石蕊溶液变成红色(答出前后两点得2分,只答出一点得1分) (3)低蜡烛先熄灭,随后高处的蜡烛熄灭二氧化碳密度比空气大,不可燃也不支持燃烧 33.(6分)[改进与实验](1)没有接触到氧气(2)温度未达到红磷的着火点 [反思与评价] (1)防止白磷燃烧生成的五氧化二磷逸散到空气中,造成污染(2)B、C [拓展与迁移] 1/5,氧气约占空气总体积的1/5 四、计算题(共7分) 34.(4分)6.5g 35.(3分)(1)2.2g (2)经计算,碳酸钠的质量分数为96.4%,与包装说明不符 (责任编辑:admin) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||