张家港市凤凰中学2005-2006学年第一学期初三化学期末模拟试卷
http://www.newdu.com 2025/11/07 06:11:37 人民教育出版社 佚名 参加讨论
张家港市凤凰中学2005-2006学年第一学期初三化学期末模拟试卷 第1卷 选择题 (共38分) 一、选择题:以下各题,只有一个符合要求的答案。 1.下列俗语或成语所涉及的内容,有一项与化学变化或化学性质无关。它是( ) A.铁杵成针 B.蜡炬成灰 C.烈火成金 D.海枯石烂 2.人类生活需要能量。下列能量主要由化学变化产生的是( ) A.电熨斗通电发出的热量 B.电灯通电发出的光 C.水电站利用水力产生的电能 D.液化石油气燃烧放出的热量 3.“绿色化学工艺”是消除污染的重要手段,其理想工艺是反应物里的原子全部转化到欲制取的物质中。下列化学反应类型一定属于“绿色工艺”的是 ( ) A.置换反应 B.分解反应 C.化合反应 D.氧化反应 4.NO是大气污染物之一,但少量NO在人体内具有扩张血管、增强记忆的功能。NO难溶于水,通常条件下极易与氧气反应。实验室收集NO的装置是( ) 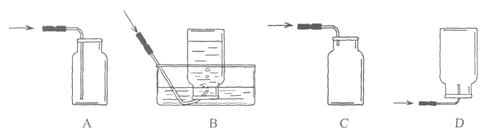 5.下列日常生活中的物质在混合后不能形成溶液的是( ) A.少量味精放入水中 B.奶粉放入沸水中 C.蜂蜜放入水中配成饮料 D.食用油滴入汽油中 6.月球土壤含有大量氦原子,它可能成为未来核能的重要原料。氦原子核内有2个质子和1个中子。氦原子结构示意图是( )  7.乙烯(化学式为C2H2)常用于水果催熟。下列说法正确的是( ) A.乙烯的相对分子质量为13 B.乙烯中碳元素与氢元素的质量比为1:2 C.乙烯的相对分子质量为26 g D.乙烯中碳元素与氢元素的质量比为12:1 8.洗涤剂能洗去餐具上的油污是因为洗涤剂( ) A.有乳化功能 B.可溶解于水 C.可以溶解油污 D.可以稀释油污 9.生活中的下列现象不能说明气体溶解度随温度升高而减小的是( ) A.烧开水时,沸腾前有气泡逸出 B.喝下汽水感到有气体冲出鼻腔 C.揭开啤酒瓶盖,有大量的泡沫溢出 D.夏季黄昏,池塘里的鱼常浮出水面 10.用质量分数为5%的氯化钠溶液配制50g质量分数为1%的氯化钠溶液,必不可少的一组仪器是( ) A.托盘天平、药匙、玻璃棒 B.量筒、烧杯、酒精灯 C.量筒、烧杯、玻璃棒 D.量筒、玻璃棒、漏斗 11.下列变化不属于化学变化的是( ) A.将煤隔绝空气加热以获得焦碳、煤焦油、焦炉气 B.植物的光合作用 C.将石油加热炼制成汽油、煤油、柴油等 D.煤和石油的形成过程 12.在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化: 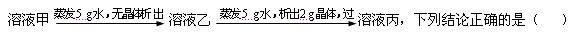 A.溶液甲可能是饱和溶液 B.溶液乙一定是不饱和溶液 C.溶液乙和溶液丙中的溶质质量分数可能相等 D.溶液丙若再蒸发5g水,析出的晶体一定大于2 g 13.冬天,人们常用甘油溶液护肤,使皮肤保持湿润。质量分数为80%的甘油溶液护肤效果最佳。配制80%的甘油溶液500 g,所需甘油的质量为( ) A.80 g B.40 g C.400 g D.100 g 14.下面有关报道,不符合科学事实的是( ) A.疏通煤气管道时,充入氩气引起火灾并发生爆炸 B.梅雨季节,一内部被虫蛀空的老柳树突然起火,烧毁 C.有易燃、易爆物的工作场所,严禁穿化纤衣物 D.一老汉因拉亮电灯,寻找煤气漏气处而引发大火,并引起爆炸 15.扑灭图书档案、贵重设备、精密仪器等火灾,不会留下任何痕迹而使物品损坏,最适宜的灭火器具是( ) A.高压水枪 B.液态二氧化碳灭火器 C.干粉灭火器 D.泡沫灭火器 16.某反应A+2B=C,若有15 g A和一定量的B恰好完全反应,生成35 g C,则参加反应的B物质的质量为( ) A.20g B.10g C.15g D.无法计算 17.从防止空气污染考虑,下列实验应在通风橱中进行的是( ) A.碘的受热和冷却 B.白磷的燃烧 C.电解水 D.白磷燃烧前后质量测定 18.10 g高锰酸钾加热一段时间后,冷却称固体残留物质量为9.2 g,则参加反应的高锰酸钾的质量为( ) A.0.8 g B.10 g C.7.9 g D.8.5 g 19.a g A 物质与b g B物质发生化合反应生成C物质,则C的质量为( ) A.等于(a+b)g B.小于(a+b)g C.大于(a+b)g D.不大于(a+b)g 第Ⅱ卷(共62分) 二、填空题 20.试简答或解释下列生活现象: (1)春暖花开的季节里,人们在公园常能闻到怡人的花香,这说明 。 (2)为了便于运输和使用,通常将石油气加压变成液态储存在钢瓶中,这一事实说明 。 (3)维生素C在酸性环境中比较稳定,受热时易被破坏,因此采用 的食用方法,才能充分利用黄瓜中丰富的维生素C。 (4)冬天人们常在汽车的水箱中加入少量乙二醇之类的化合物,目的是为了 。 (5)扑灭森林大火时设置隔离带。理由是 。 21、用化学符号表示: 镁离子 、两个氧离子 、两个氮原子 、两个氧分子 、碳酸钠 、氧化铁 、硫酸根离子 、两个硫酸分子 、氯化钠中的阴离子 、氧化铝 、两个碳酸分子 、氯原子结构示意图 。 硫酸在水中的电离方程式 、 在氯化钠溶液中存在的微粒 。 22.物质的变化过程中伴随着能量的变化。化学变化中通常伴随着能量转化,这是因为不同的物质所具有的化学能不同,在化学变化中物质具有的化学能可以转变为热能、光能或电能等。 (1)举出一个环境中吸收热能的物理变化的例子 。 (2)镁条燃烧时,化学能转化为 能和 能。 (3)已知氢气在氧气中燃烧生成水的变化放出热能。根据能量守恒原理,反应前氢气和氧气的混合物所包含的化学能比反应后化学能 (填“高”或“低”),理由是 。 23.金属材料在生活中普遍使用。铁制品表面的锈要及时除去,这是因为铁锈 会加快铁制品的生锈。铝制品不需要除锈,这是因为铝表面能形成 可以阻止铝进一步氧化。 24.根据氢气、一氧化碳、二氧化碳和甲烷四种气体的性质,试在以下的用途中各选填一种对应气体的化学式。 (1)具有还原性,可用于冶炼金属的化合物是 ; (2)可供家庭用的气体化石燃料的主要成分 ; (3)加压降温后的固体可用作制冷剂的是 ; (4)燃烧产物无污染、未来可作高能燃料的是 。 25.用“>”、“=”、“<”填写: (1)50 ℃时熟石灰的溶解度 20 ℃时熟石灰的溶解度; (2)生铁的含碳量 钢的含碳量; (3)20 ℃时氯化钠的溶解度为36 g,则20 ℃时氯化钠的饱和溶液中溶质的质量分数 36%; (4)100 g无水酒精敞口放置于空气中,一段时间后,溶液的质量 100 g; (5)质量分数为10%的蔗糖溶液100 g,取出50 g,剩下溶液的质量分数 10%;  26.在今年5月31日世界无烟日宣传活动中,某学生设计了右图所示的实验装置。该装置中的澄清石灰水可以检验香烟燃烧是否有 气体生成。为了使香烟燃烧产生的气体通过澄清石灰水,活塞应向 移动。 26.在今年5月31日世界无烟日宣传活动中,某学生设计了右图所示的实验装置。该装置中的澄清石灰水可以检验香烟燃烧是否有 气体生成。为了使香烟燃烧产生的气体通过澄清石灰水,活塞应向 移动。27.从金属的利用历史来看,先是青铜器时代,后是铁器时代,铝的利用是近100年的事。下列说法与这个先后顺序有关的是 (填写序号)。①地壳中金属元素的含量;②金属的活泼性;③金属的导电性;④金属冶炼的难易程度;⑤金属的延展性。 28、有一瓶白色粉末A,取少量用水溶解后,得到无色的溶液。向该溶液中加入适量的稀盐酸,有无色气体B放出,同时得到无色溶液C;将B通入澄清的石灰水,出现白色沉淀D;往D中加入适量的稀盐酸,又放出气体B,同时得到无色溶液E;将上述无色溶液C蒸干,最后得到食盐的晶体。根据上述实验现象,请推断有关物质的化学式:A 、B 、C 、D E 。 29.长途运输鱼苗时,人们常水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。 提出问题:当把过氧化钙投入足量水中时,最终会生成什么物质呢? 进行猜想:甲同学认为,生成氧化钙和氧气;乙同学认为,生成氢氧化钙和氧气。 (1)你认为 同学的猜想是错误的,其理由是 。 (2)请设计一个实验方案来验证另一个同学的猜想是正确的,并填入下表空格中:
30 大多数金属材料在空气中都会生锈。铜锈的主要成分是铜绿[Cu2(OH)2CO3]。某同学利用下图所示的实验一进行实验,研究铜在空气中生锈的条件。一个月后该同学发现B装置中的铜丝生锈了,而A、C装置中的铜丝无明显变化。  试回答下列问题:(1)该同学得出结论说:“铜生锈的原因是铜与空气中的氧气和水相互作用。”该同学得出的结论正确吗? ,你认为影响铜生锈的因素还可能有 。 (2)为了验证你的判断,现给你提供上图实验二所示的装置,从左到右每个仪器所盛放的试剂依次为 。 31、葡萄糖是一种有甜味、易溶于水的白色粉末状固体,化学式是C6H12O6。葡萄糖在人体内被缓慢氧化为二氧化碳和水,并释放出热量。试回答: (1)每个葡萄糖分子共有 个原子; (2)葡萄糖分子的相对分子质量 ; (3)葡萄糖中各元素的质量比为:C:H:O= ; (4)列式计算葡萄糖中碳元素的质量分数 。 32、把100 g大理石(杂质不参加反应)高温煅烧一段时间,固体质量减轻22 g,把剩下的固体加入到过量的稀盐酸中,又产生气体11 g,求此大理石中碳酸钙的质量分数。 33、根据氯化钠和硝酸钾的溶解度表,回答下列问题:
(1)写出KNO3 和NaCl具有相同溶解度时的温度范围: ;(限表中相邻两个温度之间); (2)在60 ℃时,向50 g水中加入60 g KNO3,充分搅拌后所得溶液质量为多少? (3)20℃时,200 g溶质的质量分数为20%的氯化钠溶液加热蒸发掉60 g水后降温至20 ℃,试求此时从溶液中析出的氯化钠的质量。 参考答案 (责任编辑:admin) |