2007年湖北省宜昌市初中毕业生学业考试
http://www.newdu.com 2025/12/21 08:12:01 人民教育出版社 佚名 参加讨论
2007年湖北省宜昌市初中毕业生学业考试 第I卷(选择题) 一、我会选择(本题共16小题。每小题只有一个选项符合题意。1~12题,每小题2分;13~16题,每小题3分,共36分) 1.下列变化属于物理变化的是 A.湿衣晾干 B.食物腐烂 C.纸张燃烧 D.钢铁生锈 2.日常生活中所见到的“加碘食盐”、“含氟牙膏”、“高钙牛奶”、“补铁酱油”中的“碘、氟、钙、铁”应理解为 A.原子 B.离子 C.分子 D.元素 3.生活离不开水,下列各种“水”,属于纯净物的是 A.矿泉水 B.蒸馏水 C.红墨水 D.自来水 4.下图所示实验基本操作错误的是   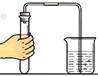  A.倾倒液体 B.读取液体体积 C.检查气密性 D.稀释浓硫酸 5.造成酸雨的主要物质是 A.SO2和NO2 B.SO2和CO C.CO和CO2 D.CH4和CO 6.“喜旺”酸奶中含有乳酸,其化学式为C3H6O3。乳酸具有帮助消化、增进食欲的功能。下列关于乳酸的说法错误的是 A.乳酸是一种有机物 B.乳酸由碳、氢、氧三种元素组成 C.一个乳酸分子共含有12个原子 D.乳酸中碳、氢、氧元素的质量比为3 : 6 : 3 7.“生命可贵,安全第一”。下列采取的安全措施错误的是 A.厨房煤气管道漏气,立即关闭阀门并开窗通风 B.自来水厂给饮用水消毒,可使用硫酸铜 C.做甲烷燃烧实验前,应先检验甲烷的纯度 D.进入久未开启的菜窖,先用蜡烛做灯火实验 8.将锌粉和铜粉放入硝酸银和硝酸镁的混合溶液中,经反应完毕后过滤。小强对所得滤液中组成物质的判断,正确的是 A.可能有硝酸银和硝酸镁 B.一定没有硝酸银和硝酸铜 C.可能有硝酸银和硝酸铜 D.一定有硝酸锌和硝酸铜 9.对下列实验指定容器中的水,其解释没有体现水的主要作用的是
10.以下是小丽做过的小实验,我认为不能成功的是 A.用蜡烛制取少量的炭黑 B.用碎鸡蛋壳和食醋制取少量CO2 C.用肥皂水区别硬水和软水 D.用孰石灰区分氯化铵和硝酸铵 11.硒元素(Se)具有防癌、抗癌作用。某饮料中含有H2SeO3,则硒元素的化合价为 A. 12.某物质可发生如下反应:2 + 2H2O === 4KOH + O2↑,则 中的物质应为 A.KO B.K2O C.K2O2 D.KO2 13.2007年“6·5”世界环境日中国主题及标识图如右,下列措施不符合这一主题的是  A.为使农作物高产,超量施用化肥和农药 A.为使农作物高产,超量施用化肥和农药B.工厂“三废”和生活污水处理达标后再排放 C.大力开发水能、太阳能等清洁能源 D.大力推广汽车使用乙醇汽油 14.下列反应不属于置换反应的是 A.Fe+CuSO4===Cu+FeSO4 B.3CO+Fe2O3 C.2F2+2H2O===O2+4HF D.2KClO3+I2===2KIO3+Cl2↑ 15.把100 g质量分数为98%的浓硫酸稀释为质量分数为10%的稀硫酸,需加水 A.980 g B.882 g C.880 g D.98 g 16.小丽同学对所学部分化学知识归纳如下,其中有错误的一组是
第Ⅱ卷(非选择题) 我要注意:1.认真审题,仔细检查;字迹工整,化学符号书写规范。 2.答案可采用文字或表格或图示等形式表达。 3.答题中可能用到的数据和资料: (1)相对原子质量:H~1 C~12 N~14 O~16 Ca~40 (2)20℃时部分酸、碱、盐的溶解性:
17.(3分)用化学符号表示下列意义: ⑴ 2个氢原子 ;⑵ 5个五氧化二磷分子 ; ⑶ 科学家最新研究发现,碳70在一定条件下吸收可见光后可高效杀灭癌细胞,有望成为癌症治疗药物的候选材料。碳70分子由70个碳原子构成,呈橄榄球状。则碳70的化学式为 。  18.(4分)化学知识在生产、生活中有广泛的应用。 18.(4分)化学知识在生产、生活中有广泛的应用。⑴ 时下兴起的环保炭雕工艺品(如右图果子狸炭雕),是以活性炭为原料,采用传统手工雕刻而成。炭雕工艺品既能装饰居室,又对甲醛等有害气体具有很强的 作用,能有效、持续地净化室内空气。 ⑵ 2008年北京奥运正在向我们走来,奥运火炬所用的燃料是丙烷(化学式:C3H8),丙烷在空气中完全燃烧的化学方程式为 。 19.(3分)右图是我们正常人每天应摄取各类营养物质的食物金字塔。 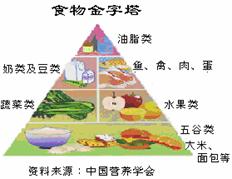 ⑴ 位于塔底的五谷类是人体每天应摄取最多的,它含有的营养素最多的一种是 ,它主要为人体机体活动和维持体温提供所需的 。 ⑴ 位于塔底的五谷类是人体每天应摄取最多的,它含有的营养素最多的一种是 ,它主要为人体机体活动和维持体温提供所需的 。⑵ 某校食堂中餐食谱如下: 主食:大米饭 配菜:红烧肉、煎鸡蛋、炸鸡腿、豆腐汤 考虑到各种营养成分的均衡搭配,应该增加的配菜是 。 20.(6分)化工生产中可用稀盐酸除去铁制品表面的铁锈。实验课上,小强将生锈铁钉放入稀盐酸中,观察到铁锈逐渐溶解,并伴有少量气泡产生,溶液由无色逐渐变为黄色,除去铁锈的化学方程式为 。 当铁钉表面没有气泡产生时,小强看到溶液仍为黄色。 再过一段时间后,小强意外发现黄色溶液逐渐变成了浅绿色。经仔细分析,小强大胆地写出溶液颜色发生改变的化学方程式为 。
21.(4分) 下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表我能回答:
⑴ 50℃时,硝酸钾的溶解度为 g。 ⑵ 由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度,则该溶解度可能是 g。 ⑶ 在60 ℃时,100 g水中加入120 g硝酸钾,充分搅拌后所得溶液质量为 g。 ⑷ 欲从海水中获得氯化钠晶体,应采取 的方法。 22.(9分)实验室常用下列装置制取气体,我能根据所学知识回答下列问题。 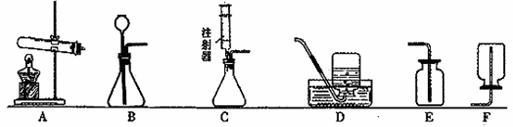 ⑴ 用A装置制取某种气体的一个化学方程式为 。 ⑵ 实验室用过氧化氢溶液和二氧化锰粉末混合制取氧气,我不选B而选用C做气体发生装置,其优点是 。 ⑶ 汽车尾气中的一氧化氮是一种大气污染物。它是一种无色气体,难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体。实验室中制取一氧化氮采用的收集装置是(填序号) 。 我认为选择气体收集方法,从气体性质的角度需要考虑的因素是: , 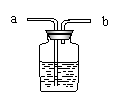 ⑷ 在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似右图所示的装置,在装置中盛放大约半瓶蒸馏水,导气管 (填“a”或“b”)端连接在供氧气的钢瓶上,该装置的作用有(填写一条) 。 ⑷ 在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似右图所示的装置,在装置中盛放大约半瓶蒸馏水,导气管 (填“a”或“b”)端连接在供氧气的钢瓶上,该装置的作用有(填写一条) 。
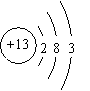 23.(11分)铝是当前应用最广泛的金属材料之一,铝的化合物在日常生活和工农业生产中也有着重要的用途。 23.(11分)铝是当前应用最广泛的金属材料之一,铝的化合物在日常生活和工农业生产中也有着重要的用途。⑴ 在地壳中,铝是含量最多的金属元素。右图是铝的原子结构示意图,铝原子的核电荷数为 ,在化学反应中容易(填“得到”或“失去”) 电子,形成铝离子(填符号) 。 ⑵ 宜昌市桥边镇建有一座铝冶炼厂,该厂以氧化铝为原料,在熔融状态下电解生成铝和一种常见的气体,其反应的化学方程式为 。 ⑶ 在日常生活中,家里防盗铁网上常刷一层“银粉”漆,其实“银粉”就是金属铝粉;铝也可用来制导线;盛装饮料的易拉罐和家用高压锅是用铝合金制造的;铝合金还应用于飞机制造上……作为材料,我发现它们具有以下优良性能(各答一条,不雷同)铝: ;铝合金: 。 ⑷ 铝的化合物氢氧化铝[Al(OH)3]是药物胃舒平的有效成分,可用于治疗胃酸过多,治疗原理用化学方程式表示为 。 24.(5分)整理、归纳物质性质之间的相互联系,是化学学习的一种有效方法。小丽在复习单质、氧化物、酸、碱、盐性质时,构建了以下知识网络图,图中短线“——”表示相连的两种物质能在一定条件下发生反应。我能帮小丽在单质、氧化物、酸、碱、盐五类物质中分别选取一种物质,将它们的化学式填写在下图圆圈中,并符合以上要求。 
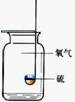
 25.(12分)一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力。小强在回顾整理下列实验中提炼了许多探究方法。 25.(12分)一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力。小强在回顾整理下列实验中提炼了许多探究方法。实验一、探究分子在不断运动(如右图) 实验现象: 。 该实验的探究方法是:对看不见、摸不着的粒子,要“观察”它的运动可以设计实验,通过宏观的现象来间接认识。 实验二、探究二氧化碳与水的反应(取四朵用紫色石蕊溶液染成紫色的干燥的小花,进行下图所示实验)  实验现象: (I)、(IV)中的小花变红。 设计(Ⅱ)、(Ⅲ)实验的目的是: 。 该实验的探究方法是:设计分析 (填“A”或“B”或“C”,获得结论。 A.仅一个单因素的实验 B.有多种因素的对比实验 C.用前面实验的生成物继续实验 实验三、验证二氧化碳与氢氧化钠溶液确实发生了反应(实验如下表所示)
我能写出实验三中方案2所涉及到的一个化学方程式 。 我认为方案1的探究方法是 , 方案2的探究方法是 。 小结:上述三个实验告诉我们:当某些化学反应现象不明显或不足以说明问题时,要千方百计通过设计出具有明显现象的实验,来准确推知和认识化学反应。
26.(2分)尿素是一种优质的氮肥,其化学式为CO(NH2)2,据此我能计算: ⑴ 尿素的相对分子质量为 ; ⑵ 一袋50 kg的尿素中氮元素的质量是 kg(保留一位小数)。 27.(5分)碳酸钙是牙膏中一种常用的磨擦剂,可用石灰石作原料来制备。宜昌市某牙膏厂现有一批石灰石样品,小丽为探究所含碳酸钙的质量分数,称取500 g样品,磨成粉末后,放在电炉上高温煅烧至质量不再发生变化,称量剩余物质量为302 g。 (有关反应的化学方程式为:CaCO3 据此我能计算: ⑴ 生成二氧化碳的质量; ⑵ 此石灰石样品中碳酸钙的质量分数。  2007年湖北省宜昌市初中毕业生学业考试化学试题 参考答案及评分说明 一、我会选择(本题共16小题。每小题只有一个选项符合题意。1~12题,每小题2分; 13~16题,每小题3分,共36分。答案用字母编号表示,每小题只选一个答案且正确得分,其它情况不得分)
二、我会填空(共4小题,化学方程式每空3分,其余每空1分,计16分。书写化学方程式时,只要化学式有错误,该空不得分;如化学式均正确,未配平或未注明反应条件或未注明状态符号共扣1分。下同) 17.⑴ 2H ⑵ 5P2O5 ⑶ C70 18.⑴ 吸附 【说明:化学名词,如字写错,该空不得分。下同】 ⑵ C3H8+5O2 19.⑴ 糖类 能量(或热量) ⑵ 青菜 【说明:填蔬菜或水果或蔬菜、水果具体名称也可。】 【说明:对上述开放性题的解答,只要符合题意要求,均可得分。下同】 20.Fe2O3+6HCl===2FeCl3+3H2O Fe +2FeCl3===3 FeCl2 三、我会说明(共2小题,化学方程式每空3分,其余每空1分,共13分) 21.⑴ 85.5 ⑵ 36.1(或36.2) ⑶ 210 ⑷ 蒸发溶剂(或蒸发结晶或蒸发) 【说明:⑵中只要答案大于36.0小于36.3,均可得分】 22.⑴ 2KMnO4 ⑵ 控制反应的速率 ⑶ D 气体的溶解性和密度 气体与水和空气成分是否反应 ⑷ a 观察是否有氧气输出(或者观察输出氧气的速率或增加氧气的湿度……)。 四、我会分析(共2小题,化学方程式每空3分,其余每空1分,共16分) 23.⑴ 13 失去 Al3+ ⑵ 2Al2O3 ⑶ 抗腐蚀(或良好延性或良好导电性……) 密度小(或质轻或硬度高或强度大或易于加工……) ⑷ Al(OH)3 +3 HCl===AlCl3+3H2O 24.(答案示例如下)
【说明:每条连线1分。所填物质类别有相同时,按正确率高的一种物质的反应连线计分;填物质名称不得分。本题属开放性解答,其它答案合理即可给分。】 五、我会设计(共1小题,化学方程式每空3分,其余每空1分,共12分) 25.实验一 B烧杯中的无色酞酚溶液变红 实验二 验证水和二氧化碳分别是否能使紫色石蕊变色 B 实验三
CO2+2NaOH=Na2CO3+H2O(或Na2CO3+2HCl=2NaCl+H2O+CO2↑或BaCl2+Na2CO3==BaCO3↓+2NaCl或Ca(OH)2+Na2CO3==CaCO3↓+2NaOH或 CaCl2+Na2CO3==CaCO3↓+2NaCl或 Ba(NO3)2+Na2CO3==BaCO3↓+2NaNO3……) 【说明:所写步骤、现象要匹配,所写化学方程式要与上述方案相关。其它答案合理均可】 方案1:通过密闭容器内气体压强变化程度的对比来判断反应的发生(或通过反应物量的减少来判断反应的发生。) 方案2:通过验证生成物的存在来判断反应的发生。 六、我会计算(共2小题,共7分) 26.⑴ 60 ⑵ 23.3 27.解: ⑴ 根据质量守恒定律,二氧化碳的质量为:500 g-302 g = 198 g ……………………1分 ⑵ 设500g石灰石样品中碳酸钙的质量为x。 CaCO3 x 198 g 此石灰石样品中碳酸钙的质量分数为: 答:⑴ 生成二氧化碳的质量为198 g。⑵此石灰石样品中碳酸钙的质量分数为90%。……1分 【说明:设、答齐全共1分,缺一项不得分。其它合理解答,也可分步得分。】 (责任编辑:admin) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

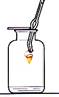
 探究燃烧的条件
探究燃烧的条件