北京市崇文区2008—2009学年度第二学期初三化学统一练习(二)
http://www.newdu.com 2025/11/06 02:11:18 人民教育出版社 佚名 参加讨论
北京市崇文区2008—2009学年度第二学期初三化学统一练习(二) 司志书(供稿) 资料:1.可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 Ca-40 Cu-64 2.部分碱和盐的溶解性表(20℃):
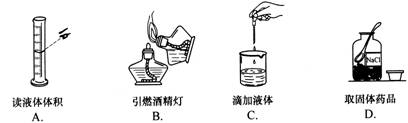
一.选择题(每小题只有1个选项符合题意。共25个小题,每小题1分,共25分。) 1.在生产生活中常用到下列物质,属于纯净物的是 A.食盐水 B.不锈钢 C.水 D.牙膏 2.下列物质中存在氧分子的是 A.二氧化碳 B.空气 C.高锰酸钾 D.氧化汞 3.能保持氢气化学性质的粒子是 A.H B.H2O C.H+ D.H2 4.以下事实,不能说明分子间有间隔的是 A.海绵能吸水 B.用打气筒能将气体压缩 C.物体有热胀冷缩的现象 D.酒精和水混合后,总体积小于两者的体积之和 5.不同元素本质的区别是原子的 A.电子数不同 B.中子数不同 C.质子数不同 D.最外层电子数不同 6.早在三年前,北京就推出“单车总动员”迎奥运首都公共自行车行动。许多市民也开始不开汽车,改骑自行车上班。从环保角度看,这主要是有利于减少城市的 A.大气污染 B.水污染 C.土壤污染 D.白色污染 7.下列符号既能表示某种元素,又能表示该元素的一个原子,还能表示一种物质的是 A.SO2 B.O2 C.N D.Cu 8. 下列四种化肥中,属于复合肥料的是 A.KCI B.NH4C1 C.NH4NO3 D.KNO3 9.有机合成材料的出现是材料发展史上的一次重大突破。下列属于合成纤维的是 A.棉花 B.涤纶 C.蚕丝 D.羊毛 10.分别将下列各物质加入到足量水中,能得到无色、澄清溶液的是 A.NaCl B.CuSO4 C.CaCO3 D.FeCl3 11.对于化学方程式:6Fe+3O2 A.该反应不能发生,因为不符合客观事实 B.反应物、生成物的化学式书写错误 C.反应条件不正确 D.没有遵守质量守恒定律(没有配平) 12.下列实验操作正确的是
  13.右图是元素周期表中的一格,能从该图获取的信息是 13.右图是元素周期表中的一格,能从该图获取的信息是
14.下列能源在使用的过程中,可能会引起酸雨的是 A.煤 B.风能 C.氢能 D.太阳能 15.下列物质的用途主要利用物质的物理性质的是 A.碳酸氢钠用于治疗胃酸过多 B.大理石用作建筑材料 C.盐酸用于除铁锈 D.熟石灰用于改良酸性土壤 16.下列有关空气中各成分的说法,正确的是 A.氮气的化学性质不活泼,可在食品包装时充入防腐 B.氧气化学性质比较活泼,能燃烧 C.二氧化碳能产生温室效应,因此属于空气污染物 D.稀有气体一定不与其他物质发生化学反应 17.高铁酸钾(K2FeO4)是一种新型高效水处理剂。下列关于该物质的叙述,正确的是 A.它是一种氧化物 B.组成中含有两种非金属元素 C.它是一种混合物 D.K2FeO4中铁元素的化合价为+6学科网 18.我国有辽阔的海岸线,有充足的海水资源。人们常把海水引入盐田,经过风吹日晒使海水中的水分蒸发获得粗盐。在此过程中 A.溶剂的质量不变 B.氯化钠的质量不变 C.氯化钠的质量分数始终不变 D.氯化钠的质量分数变小 19. “节能减排,我有责任”。下列实验操作不符合节约原则的是 A.甲学生用白色点滴板代替试管,进行酸、碱溶液与指示剂反应的实验 B.乙学生配制50g 5%的氯化钠溶液,把配好的溶液装入试剂瓶,盖好瓶塞,贴标签备用 C.丙学生用氯酸钾和二氧化锰制氧气时,先点燃酒精灯,再去组装仪器 D.丁学生做完金属与酸的反应实验后,把多余的金属和剩余的溶液回收 20.下列有关叙述正确的是 A.糖类和油脂都能为人体提供能量 B.人体缺钙易引起食欲不振 C.合成纤维、塑料、合金等都属于合成材料 D.青少年生长过程需要大量蛋白质,所以要多吃水果 21.下列说法正确的是 A.有单质参加的反应一定是化合反应 B.稀溶液一定是不饱和溶液 C.任何物质的溶解度都随温度升高而增大 D.在化合物理,元素正价总数和负价总数的绝对值相等 22.归纳物质的性质能够找出它们之间的内在联系,如物质之间的共性(即相同的性质)或特性(即不同的性质)。下列各组物质的共性和特性的叙述,错误的是
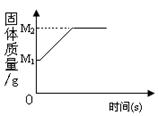 23.一定质量的镁带在氧气中完全燃烧后生成氧化镁,其固体质量随时间的变化可用右图表示,则用(M2-M1)表示的质量是 A.生成MgO的质量 B.参加反应的Mg的质量 C.参加反应的O2的质量 D.剩余的O2的质量 24.2008年底,美国《科学》杂志评出年度十大科学突破,排名第六的是可以“燃烧的水”。美国科学家称已开发出一种新的廉价催化剂,可利用电能将水分解。下列有关说法不正确的是 A.水在通电的条件下可分解成氢气和氧气 B.水电解产生氢气和氧气的体积比为2∶1 C.美国科学家的突破是利用廉价催化剂使水直接燃烧 D.以水为原料廉价地获得氢能源,可以有效地缓解温室效应 25.只含铜、氧两种元素的固体样品9.0g,测得其中含铜元素的质量为8.0g。已知铜有CuO和Cu2O两种氧化物,且均为固体。下列说法不正确的是 A.固体样品可能是Cu2O B.固体样品的物质成分组合只有2种情况 C.固体样品可能是Cu、CuO与Cu2O的混合物 D.若固体样品中只含两种物质,则两种物质的质量比可能为5︰4 二.填空题(每空1分,共30分) 26.(8分)请将五氧化二磷的化学式填在下表中相应的位置,并根据下表回答有关问题:[除(3)外,各小题均用序号填空]
(1)表中的物质属于单质的是 ,属于有机物的是 。 (2)表中的物质可用于人工降雨的是 ,可用于制肥皂、造纸等工业的碱是 。 (3)写出甲烷燃烧的化学方程式 。 (4)若要测定某烧碱溶液的酸碱度,不能选用下列选项中的 。 ①无色酚酞溶液 ②紫色石蕊溶液 ③pH试纸 (5)我国福建生产一种槟榔芋,芋皮上含有一种碱性的物质——皂角素,皮肤沾上它会奇痒难忍。你认为可选用下列中的 来涂抹止痒。 ①食醋 ②熟石灰 ③肥皂水 ④柠檬汁 27.(4分)阅读材料,回答问题。  材料:2000年悉尼奥运会,生物学家邓肯在4米深的水下手擎火炬潜泳3分钟,利用镁在氧气中燃烧,创造了“水火交融”的奇观,实现了火炬的水下传递(见右图)。 (1)物质燃烧的三个条件是:① ;② ;③达到燃烧所需的最低温度。 (2)分析火炬在水中燃烧的情况,请回答: ①火炬中镁在氧气中燃烧的化学方程式为 。 ②水中火炬能保持燃烧所需的最低温度的原因是 。 28.(4分)车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料。 (1)乙醇属于 能源,使用乙醇汽油可节省石油资源。 (2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W。现测得反应前后各物质的质量如下:
①根据质量守恒定律,得出表中x的值为 ; ②根据表中数据,可确定未知物W中所含元素及各组成元素的质量比为 ; (3)为了使乙醇汽油燃烧过程中少产生 W,应采取的措施是 (任写一种)。 29.(9分)钢铁是重要的金属材料。 (1)目前世界上已有50%以上的废旧钢铁得到回收利用,其目的是 (填字母序号)。 A. 节约金属资源 B. 合理开采矿物 C. 防止钢铁生锈 (2)高层建筑的楼顶常装有用钢铁做的避雷针,其作用是将雷电引导到地下,这说明钢铁具有良好的 性(填一物理性质)。处于楼顶的避雷针生锈了,铁生锈需要的条件是要有 (填名称)的参与。 (3)为防止水龙头生锈,可以采取的措施有 (任写一种)。 (4)将生锈的铁制品放入盛有稀盐酸的洗槽中,观察到溶液由无色变为黄色。写出此反应的化学方程式 。 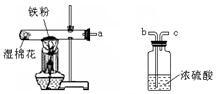 (5)某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样一个实验:让水蒸气通过一根烧红的铁枪管,生成了一种气体。同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应? 生成的气体又是什么? 带着这些疑问,他们设计了如右图所示的装置进行探究。 ①已知试管内棉花不参加化学反应,它的作用是 ; ②若干燥从a导管出来的气体,应从 (选填“b”或“c”) 端管口通入; ③对化学变化过程中生成的气体,同学们有以下猜想: 猜想一:生成的气体可能是氧气 猜想二:生成的气体可能是 。 ④红热的铁遇到水蒸气,在生成气体的同时,还会生成一种黑色固体。你认为生成的黑色固体可能是 。 30.已知A~N是初中化学常见的12种物质,其中H是由四种元素组成的化合物。反应①、②、③、④、⑤中有四个反应分别属于四个基本反应类型中的一种(反应条件已略去)。 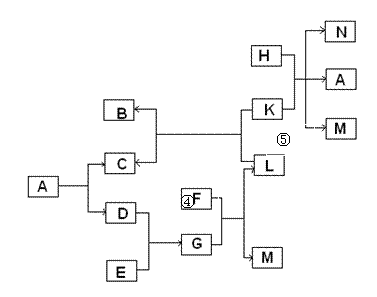 (1)写出物质的化学式:B ,E 。 (2)写出反应①、③、⑤的化学方程式:① ;③ ;⑤ 。 三.实验题(每空1分,共19分) 31.(6分)(1)实验室中常用高锰酸钾受热分解制取氧气。 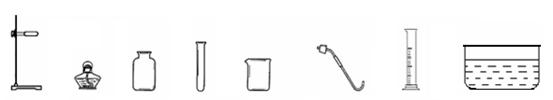 a b c d e f g h ①写出该反应的化学方程式_____。 ②组装制取氧气装置,从上图中选择所需的仪器有_____(填字母序号)。 ③装置组装完成后,装药品前应首先进行的操作是 。 (2)根据下列实验回答: 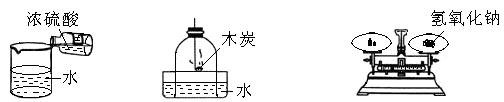 A.稀释浓硫酸 B.空气中氧气含量的测定 C.称取一定质量的氢氧化钠固体 ①图A中的操作错误是 。 ②用图B的方法测定空气中氧气的体积分数,会使结果偏低,改进的措施是 。 ③图C称量氢氧化钠固体的方法有 处错误。 32.(4分)用含有少量生石灰的NaCl固体,配制一定质量分数的NaCl溶液。实验步骤如下图所示: 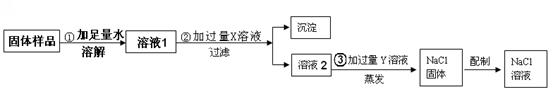 (1)溶液1中所含溶质为 (填化学式)。 (2)加入X发生反应的化学方程式为 。 (3)加入的Y为 (填化学式),所发生反应的化学方程式为 。 33.(9分)实验室里的同学们正在做探究实验。用A、B、C、D四支试管各取室温下等体积的氢氧化钙饱和溶液,分别做如下实验:①向A试管中滴加碳酸钾溶液;②向B试管中滴加氯化铜溶液;③向C试管中滴加硝酸镁溶液;④向D试管中滴加氯化钠溶液,均充分振荡。 (1)提出问题:他们在探究的问题是 (请具体回答)。 (2)表达与交流:小芳根据在D试管中没有观察到明显现象,判断D试管中无化学反应发生。你认为此判断的依据是否合理 (填“合理”或“不合理”),并具体解释原因 ; (3)为科学处理实验过程中产生的废液,同学们对B试管中反应后过滤得到的无色滤液,继续进行探究。小芳猜想滤液中只含有一种溶质,小刚猜想滤液中含有两种溶质。为验证哪位同学的猜想是正确的,同学们选用不同的试剂分别进行实验。请填写下列实验报告:
(4)反思与评价:通过上述实验,同学们认为实验过程中产生的废液必须处理后再排放。 请你对B试管中滤液的处理提出可行的建议 。 四.计算题(共6分,计算结果均保留一位小数) 34.工业上高温煅烧含碳酸钙90%的石灰石(杂质高温不分解),可制得氧化钙和二氧化碳。如果要制取5.6 t的氧化钙,需要石灰石多少吨? 35.甲、乙、丙三位同学用下列试剂分别进行实验,所取试剂用量如下表所示,且反应均恰好完全。
已知:A1+A2+A3 = 23.0g , B1+B2+B3 = 219.0g , 现将甲、乙、丙三位同学所得到的溶液倒入同一容器中,所得溶液总质量为237.6g。求: (1)丙同学所取CaCO3固体的质量; (2)最终所得混合溶液中溶质的质量分数。 参考答案及评分标准 一.选择题(每小题只有1个选项符合题意。共25个小题,每小题1分,共25分。)
二.填空题(每空1分,共30分) 26.(8分)P205 (1)② ① (2)④ ③ (3)CH4+2O2  2H2O+CO2: 2H2O+CO2:(4)①② (5)①④ 27.(4分)(1)①可燃物 ②与氧气(或空气)接触 (2)①2Mg +O2  2MgO ②镁与氧气反应放出的热 2MgO ②镁与氧气反应放出的热28.(4分)(1)可再生 (2) ①14 ②C:O = 3:4 (3)加大空气的进入量 29.(9分)(1) A (2)导电 氧气和水 (3)刷漆(或镀耐腐蚀的铬等金属、或使用合金材料等) (4)Fe2O3+6HCI == 2FeCl3+3H2O (5)①提供反应所需的水 ②b ③H2 ④Fe2O3 30.(5分)(1)FeCl2(或FeSO2) C) ①2H2O  2H2↑+O2↑ 2H2↑+O2↑③Fe2O3+3CO  2Fe+3CO2 ⑤NaHCO3 +HCI === NaCl +H2O+CO2 ↑ 2Fe+3CO2 ⑤NaHCO3 +HCI === NaCl +H2O+CO2 ↑(或2NaHCO3+H2SO4 === Na2SO4+2H2O+CO2↑) 三.实验题(每空1分,共19分) 31.(6分)(1)①2KMnO4  K2MnO4+MnO2+O2 ②abcdfh ③检查装置的气密性 K2MnO4+MnO2+O2 ②abcdfh ③检查装置的气密性(2)①没有用玻璃棒搅拌 ②将木炭换成红磷(或白磷) ③2 32.(4分)(1)Ca(OH)2和NaCl (2)Ca(OH)2+Na2CO3 === CaCO3 ↓+2NaOH (3)HCl Na2CO3+2HCI == 2NaCl+H2O+CO2 ↑和NaOH+HCl == NaCl+H2O(答完整得1分) 33.(9分)(1)氢氧化钙与各种盐的反应(此空合理答案即可得分) (2)不合理 有些化学反应无明显现象 (3)
(4)加酸中和,使溶液为中性后排放 四.计算题(共6分) 34.(3分)解:设需要石灰石的质量为x CaCO3  CaO+CO2 ↑ (1分) CaO+CO2 ↑ (1分)100 56 90%×x 5.6t 100∶90%x == 56∶5.6 t (1分) x=11.1 t (1分) 答:需要含碳酸钙90%的石灰石11.1t 。 35.(3分)解:(1)设丙同学所取CaCO3固体的质量为x 反应生成二氧化碳的质量为:23.0g + 219.0g-237.6g = 4.4g CaCO3+2HCl == CaCl2+H2O+CO2 ↑ 100 44 X 4.4g x=10.0g(1分) (2)因为都是恰好完全反应,所以溶液中的溶质是CaCl2,且CaCl2的质量可由氯元素在反应前、后守恒计算得出 设反应共生成CaCl2的质量为y 2HCI ~ CaCl2 73 111 219g×10% y y=33.3g(1分) CaCl2的质量分数: 答:(1)丙同学所取CaCO3固体的质量为10.0g; (2)最终所得混合溶液中溶质的质量分数为14.0%。 (注:此题解题方法合理,结果正确得分) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
