物质构成的奥秘 阶段测评
http://www.newdu.com 2025/11/06 05:11:50 人民教育出版社 佚名 参加讨论
物质构成的奥秘 阶段测评 (测评时间为45分钟,满分为100分) 一、选择题(每小题3分,共45分) 1.市售某药的标签上印有所含成分的说明如下:每100g药片中含碘15g,铁1.2g,镁6.5g,锌0.15g,锰0.1g。这里的碘、铁、镁、锌、锰是指( ) A.分子 B.元素 C.单质 D.化合物 2.下列各组物质,前者属于化合物、后者属于单质的是( ) A.二氧化碳、二氧化锰 B.冰水混合物、水 C.水、臭氧 D.医用酒精、蒸馏水 3.区别二氧化碳、氧气、空气三种气体,应采用的方法是( ) A.将气体分别通入水中 B.将燃着的木条分别伸入集气瓶中 C.将气体分别通入澄清石灰水中 D.分别观察颜色 4. NO是大气污染物,但少量NO在人体中具有扩张血管,增强记忆功能。NO难溶于水,通常条件下极易与 A. NO是氧化物 B. NO对人体有一定的作用 C. NO与氧气反应是它的物理性质 D. NO可用排水法收集 5.下列粒子能保持氢气化学性质的是( ) A.H B.2H C. 6.下列物质中存在氧分子的是( ) A.二氧化碳B.高锰酸钾C.水D.空气 7.原子的质量主要取决于( ) A.核外电子的质量 B.原子核内质子和核外电子的质量 C.中子的质量 D.原子核内质子和中子的质量 8.在 A.两个氢原子 B.氢元素 C.两个氢元素 D.氢分子 9.有一原子,其核电荷数为112,相对原子质量为277,下列说法错误的是( ) A.中子数和核外电子数之差为53 B.中子数为112 C.质子数和中子数之和为277 D.质子数为112 10.同种元素的原子和离子相比较,不同的是( ) A.质子数 B.中子数 C.核外电子数 D.原子核 11.“ A.二氧化碳是由一个碳元素和一个氧元素组成的 B.二氧化碳分子是由一个碳元素和两个氧元素构成的 C.二氧化碳分子是由碳原子和氧分子构成的 D.每个二氧化碳分子是由一个碳原子和两个氧原子构成的 12.一氧化氮(NO)中氮元素的化合价是( ) A.+2 B.+3 C.+5 D.+6 13.下列氯元素的化合价依一定规律排列:HCl、 A. NaCl B. HClO C. 14.下列原子结构示意图所表示的元素中,化学性质最稳定的是( ) 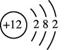 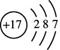 A. B. C. D. 15. 2005年3月,国家质检局查出一些辣椒酱、番茄酱等食品中含有工业用色素“苏丹红一号”,人食用后可能致癌。“苏丹红一号”的化学式为 A.“苏丹红一号”属于氧化物 B.“苏丹红一号”由30个原子构成 C.“苏丹红一号”的相对分子质量为248 D.“苏丹红一号”中氢元素的质量分数为0.4% 二、填空题(共38分) 16.(6分)用①电子;②质子;③中子;④原子核;⑤原子;⑥分子;⑦混合物;⑧纯净物;⑨单质;⑩化合物的序号填空: (1)上列粒子中带正电荷的是_____________; (2)空气、海水、白酒是不同的物质,但它们同属于______________; (3)氧原子的原子核内有8个带1个单位正电荷的_______________,核外有8个_______________在一定范围的空间里作高速运动,由于每一个_________________带1个单位负电荷,________________不带电,所以整个________________不显电性; (4)由于和的相对质量约为1,氧的相对原子质量为16,可知氧的原子核内有8个和8个。 17.(6分)下图为4种粒子的结构示意图,完成以下空白: 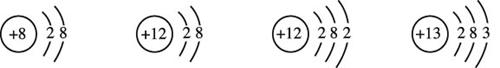 A B C D (1)属于阳离子结构的粒子是______________; (2)B粒子的电子数______________C粒子的电子数(填“大于”、“小于”或“等于”)。 18.(2分)相对原子质量约为56的A原子中有30个不带电的中子,则其质子数为____________。 19.(4分)H,D,T三种原子的原子核内质子数相同都为1,但中子数不同,它们是____________(填“同”或“不同”)种元素,它们核外的电子数______________(填“相同”或“不同”)。 20.(8分)用化学符号来表达下列物质: (1)一个硫离子____________;(2)两个铝原子_____________;(3)三个氧分子______________;(4)硫酸亚铁_______________;(5)碳酸钠____________;(6)氢氧化铜______________;(7)氧化钠_______________;(8)二氧化碳______________。 21.(12分)在宏观物质、微观粒子和化学符号之间建立联系,是化学科学特有的思维方式。已知氢、碳、氧、钠、氯五种元素的核电荷数分别为1、6、8、11、17。试按下列要求,写出微观粒子的化学符号,以及符号表示的意义或对应的物质的名称(微观粒子和物质所涉及的元素限定在上述5种元素内)。
三、计算题(共17分) 22.(5分)人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙〔
(1)包装标签上脂肪≥3.3g,是指100mL牛奶中含脂肪的质量至少3.3g。那么一盒牛奶含钙至少g(保留到0.01g); (2)求羟基磷酸钙中钙元素的质量分数(保留为0.1%); (3)若人体每天至少需要0.6 g钙,且这些钙有90%来自牛奶,则一个人每天至少要喝多少盒牛奶? 23.(12分)右图是某化肥的标签,请列式计算。
(1) (2) (3)通过计算碳酸氢铵的含氮量(氮元素的质量分数),说明此标签是否有错误; (4)若1 kg硝酸铵( |
- 上一篇:第二单元 我们周围的空气 单元测试
- 下一篇:自然界的水 单元测试