|
2013年中考化学试题汇编——溶液(三) 微山县鲁桥一中 黄尊英 41.(2013.连云港)图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图像和有关信息判断,下列说法中错误的是 ( ) 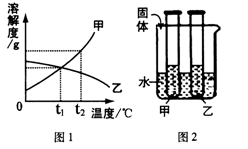 A.t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为:甲>乙 B.将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,两种溶液中溶质质量分数相等 C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小 D.向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出 42.(2013年德阳市)20℃时,取四份一定质量的饱和硝酸钾溶液进行如下实验后,所得结论正确的是( ) A.保持温度不变,减少10g溶剂后,溶液中溶质的质量分数增大 B.保持温度不变,加入10g溶质后,溶液中溶质的质量分数增大 C.保持温度不变,加入10g溶剂后,溶质的溶解度减小 D.降温至10℃后,溶质的溶解度减小 43.(2013.河北省)20 ℃时,取甲、乙、丙、丁四种纯净物各20 g,分别加入到四个各盛有50 g水的烧杯中,充分溶解,其溶解情况如下表:
下列说法正确的是 ( ) A.所得四杯溶液都是饱和溶液 B.丁溶液的溶质质量分数最大 C.20 ℃时四种物质溶解度的关系为:丙>乙>甲>丁 D.四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液 44.(2013.眉山市)如图所示,是甲、乙、丙三种固体物质的溶解度曲线。下列说法正确的是( ) 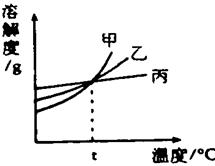 A、t℃时,甲、乙、丙三种物质的饱和溶液的质量分数相等 B、在两份相同质量的水中分别加入甲与丙,达到饱和时溶解甲的质量大于丙 C、相同温度时,甲、乙、丙三种饱和溶液,其质量分数关系为:甲>乙>丙 D、甲中混有少量丙时,可采用高温制成热的饱和溶液,再蒸发结晶提纯甲 45.(2013.呼和浩特)海洋资源开发前景广阔。海水晒盐能够得到粗盐和卤水,卤水中含有MgCl2、KCl和MgSO4等物质,下图是它们的溶解度曲线。下列说法不正确的是 ( ) 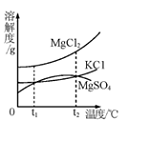 A.t1℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgCl2 B.t1℃时,分别在100g水中溶解了等质量的MgCl2、KCl ,两溶液都可达到饱和 C.t2℃时,KCl和MgSO4两种物质的溶解度相同 D.将t2℃的三种物质的饱和溶液降低到t1℃时,均能析出晶体 46.(2013.荆门市)下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( ) 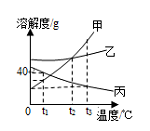 A.t2℃时,甲、乙两种物质的溶解度相等 B.甲的溶解度随温度的升高而增大 C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是 D.t1℃时,丙的饱和溶液中溶质的质量分数为40% 47.(2013.吉林省)结合下图判断,下列说法正确的是( ) 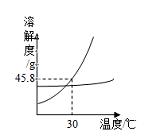 A.硝酸钾的溶解度为45.8g B.硝酸钾的溶解度大于氯化钠的溶解度 C.升高温度可将硝酸钾的不饱和溶液变为饱和溶液 D.两条曲线的交点所对应溶液的溶质质量分数相等 48.(2013.盐城市)下图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( ) 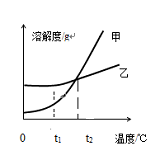 A.甲物质的溶解度一定大于乙物质的溶解度 B.t20C时,甲、乙饱和溶液的溶质质量分数相等 C.将甲溶液从t20C降温到t10C时,一定有晶体析出 D.将t20C时乙的饱和溶液变为不饱和溶液,可采用 降温的方法 49.(2013?扬州)如图是KNO3和NH4Cl的溶解度曲线.下列说法正确的是( ) 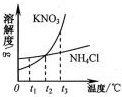 A. t1°C时,KNO3的溶解度大于NH4Cl B. t2°C时,KNO3和NH4Cl的溶解度相等 C. t3°C,两溶液中KHO3的质量分数一定大于NH4Cl D. NH4Cl的溶解度受温度的影响大于KNO3 50.(2013.绍兴市)通过如图所示的实验(不考虑水分蒸发),得到相应的五种溶液。下列叙述不正确的是( ) 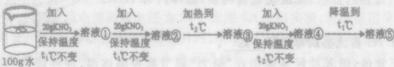 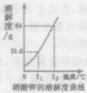 A.t1℃时,溶液①是不饱和溶液 B.t2℃时,溶液④是饱和溶液 C.t1℃时,溶液⑤是饱和溶液 D.t2℃时。溶液③是不饱和溶液 51.(2013.昆明市)在80℃时,物质A的溶解度比B小。分别取等质量的A、B两物质的饱和溶液,降温至30℃,析出A、B晶体的质量分别为mg和ng(A、B均不含结晶水)。下列判断正确的是( ) A.80℃时,A饱和溶液与B饱和溶液相比,前者所含溶质的质量一定比后者小 B.30℃时,若A的溶解度比B大,则m一定小于n C.30℃时,若A的溶解度比B小,则m一定大于n D.30℃时,A 饱和溶液与B饱和溶液相比,后者溶质的质量分数一定比前者大 52.(2013.烟台市)下图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( ) 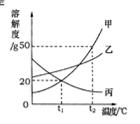 A.要配制相同质量分数的甲、丙两种物质的饱和溶液,应该将温度控制在t1℃ B.t2℃时,将30g甲物质加入到50g水中不断搅拌,形成的溶液中溶质的质量分数是37.5% C.要从甲物质的饱和溶液中获得晶体甲,可采用降温结晶的方法 D.将丙物质的饱和溶液转化为不饱和溶液可以采用加水或降温的方法 53.(2013.金华)如图是A、B两种物质的溶解度曲线,下列叙述错误的是( ) 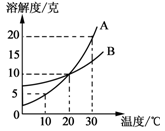 A.30℃时,向100克水中加入25克A物质,充分溶解后所得溶液是饱和溶液 B.A物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 C.B物质的饱和溶液从30℃降温到20℃,其溶质质量分数减小 D.30℃时,将B物质的不饱和溶液转变为饱和溶液,可以采取恒温蒸发溶剂的方法 54.(2013.株洲市)(6分)华雪同学想制取“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液。请回答下列问题: (1)若用氢氧化钠固体配制,需称取氢氧化钠 g。 (2)若用25%的氢氧化钠溶液配制,需25%的氢氧化钠溶液 g;蒸馏水 g;配制时应选用 mL(选填“10”、“20”、“50”、“100”)的量筒量取蒸馏水。 (3)下列操作正确的是 。 A.在托盘天平的左右托盘上垫滤纸称取氢氧化钠固体 B.将准确称取的氢氧化钠固体直接倒入装有水的量筒中溶解 C.将配制好的NaOH溶液装入玻璃试剂瓶中,塞好橡胶塞并贴上标签 (4)在实验室配制氢氧化钠溶液时, (填“要”或“不要”)用到玻璃棒。 55.(2013.泸州市)某同学用天平称取NaCl固体19g,用量筒量取蒸馏水76ml(水的密度为1g/cm3),配制一定质量分数的氯化钠溶液,该氯化钠溶液的溶质质量分数为 。若该同学量取水时是仰视读数,则所配制的氯化钠溶液溶质质量分数会 (填“偏大”、“不变”、“偏小”)。 56.(2013.眉山市)(4分)已知98﹪浓H2SO4密度为1.84g/cm3,62﹪浓HNO3密度为1.14g/cm3;若要配制浓H2SO4与浓HNO3的混合溶液,则应将 (填化学式)沿玻璃棒缓慢倒入盛有 (填化学式)的烧杯中,边加边搅拌,冷却后装瓶。过程中玻璃棒的作用是 、 。 57.(2013.泸州市)配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。 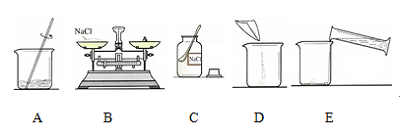 请回答下列问题: (1)用上图所示的序号表示正确配制该溶液的操作顺序为 。 (2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 。 A C.调节游码 D.添加砝码 (3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 。 58.(2013.达州市)(3分)A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题:  ⑴t1℃时,A的饱和溶液中溶质与溶液质量比 ; ⑵若B中含有少量A,应用 法提纯B; ⑶若将A的饱和溶液从t2℃降温到t1℃时,一定不会发生改变的是 。 A.溶解度 B.溶剂质量 C.溶质质量 D.溶质质量分数 59.(2013.庆阳市)(4分)如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:  (1)t1℃时,A物质的溶解度为 g; (2)a点的含义是 ;在t2℃时,A、B两物质的溶解度相同 (3)溶解度受温度影响小的物质是 ; (4)从A、B的混合物中分离A物质,一般采用 的方法。 60.(2013.南京市)若要配制245g质量分数为10%的稀硫酸,需要质量分数为98%的浓硫酸(密度为1.84g/cm3) mL(计算结果保留一位小数),由浓溶液配制稀溶液时,计算的依据是 。在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、 、混匀、冷却至室温装瓶并贴上标签。 参考答案: 41~45 BDCAB 46~50 DDBBD 51~53 BBB 54.(1)5 (2)20 30 50 (3)C (4)要 55.20% 偏小 56.浓H2SO4 浓HNO3 引流 搅拌 57.(1) CBDEA (2) B (3) 加速溶解 58.⑴S:(100+S) ⑵蒸发结晶 ⑶B 59.(1)25(2)在t2℃时,A、B两物质的溶解度相同(3)B(4)冷却热饱和溶液 60.13.6,溶液稀释前后,溶质的质量不变 量取 (责任编辑:admin) |
