|
初三化学竞赛试卷 (总分100分 时间一小时) 得分_____________ 相对原子质量:H-1、C-12、N-14、O-16、Na-23、Mg-24、Al-27、S-32、Cl-35.5、K-39、Ca-40、Fe-56、Cu-64、Zn-65、Ag-108、Ba-137、Pb-207。 一、单项选择题(共70分;每小题只有1个正确答案) 1. 吴蕴初(1891—1953)是我国现代化学工业的先驱者。20世纪20年代后,他陆续创办了一系列“天字号”化工企业,为开拓和振兴民族化工作出了重大贡献。以下由他创办的各“天字号”企业与其生产的产品不对应的是 ( ) A. 天原厂──氯碱等化工原料 B. 天厨厂──橡胶制品 C. 天盛厂──耐酸陶器 D. 天利厂──氨和硝酸 2. 下列元素符号书写有误的是……………………………………………………… ( ) A. TI B. V C. Re D. In 3. 硫酸的酸酐是………………………………………… ( ) A. H2S B. S C. SO2 D. SO3 4. 下列金属中,人类开发利用最晚的是……………………………………………( ) A. Al B. Fe C. Cu D. Au 5. 下列食物中富含淀粉的是………………………………………………………… ( ) A. 蔬菜 B. 鸡蛋 C. 大米 D. 猪肉 6. 含磷洗衣粉的使用会造成严重的环境污染,含磷洗衣粉的“磷”是指……… ( ) A. 白磷 B. 红磷 C. 甲胺磷 D. 三聚磷酸钠 7. 下列物质属于纯净物的是………………………………………………………… ( ) A. 水银 B. 含氮量为33.5%的硝酸铵样品 C. 盐酸 D. 混有金刚石颗粒的石墨样品 8. 许多物质的名称中含有“水”。“水”通常有三种含义:①表示水这种物质;②表示物质处于液态;③表示水溶液。下列物质名称中的“水”不属于以上三种含义的是 ( ) A. 重水 B. 氨水 C. 水银 D. 水晶 9. 下表列出了NO的部分物理性质和化学性质:
则实验室收集NO气体,可采用的方法是……………………………………………( ) A. 向上排空气法 B. 向下排空气法 C. 排水集气法 D. 既可用向上排空气法,又可用排水集气法 10.下列有关分子和原子的说法中,正确的是……………………………………… ( ) A. 原子是由质子和中子构成的 B. 保持水的化学性质的粒子是氢原子和氧原子 C. 分子的质量总比原子的质量大 D. 分子和原子都可以构成物质 11.欲除去热水瓶中的水垢,可采用的方法是……………………………………… ( ) A. 用食盐水洗涤 B. 用洗洁精洗涤 C. 用白酒洗涤 D. 用醋洗涤 12.铝碳酸镁是一种天然矿物,它最广泛的用途是作为新型抗酸药,用于治疗胃溃疡、胃酸过多症等,其化学式为Al2Mg6(OH)xCO3·4H2O。其中x为………………………… ( ) A. 15 B. 16 C. 17 D. 18 13.下列有关食品加工的做法不会影响人体健康的是……………………………… ( ) A. 用甲醛的水溶液浸泡海产品 B. 用碳酸氢钠焙制糕点 C. 用淀粉、蔗糖、奶香精配成奶粉 D. 用工业石蜡涂抹在瓜子表面增加光泽 14.右图是一幅贴在汽车加油站上的宣传广告。围绕这幅广告画以下叙述错误的是  …………………………………………………………………… ( ) …………………………………………………………………… ( )A. 玉米汁可用作汽车燃料 B. 由玉米生产的酒精汽油可作汽车燃料 C. 推广玉米生产的燃料可在一定程度上缓解当前的能源危机 D. 以农作物为原料来生产化学品是可行的 15.下列各组物质组成的混合物可按溶解、过滤、蒸发的操作顺序,将各组分分离的是 ……………………………………………………………………………………… ( ) A. 氧化铜和木炭粉 B. 硝酸钠和硝酸钾 C. 二氧化锰和氯化钾 D. 氧化钙和氯化钠 16.下列实验能达到目的的是………………………………………………………… ( ) A. 用酒精灯加热使水分解制取氢气 B. 用锌跟稀硫酸反应制取氢气 C. 用铝跟稀硝酸反应制取氢气 D. 用铁跟浓硫酸反应制取氢气 17.下列有关媒体的报道与化学知识不相违背的…………………………………… ( ) A. 某洗发水不含任何化学物质 B. 科研人员发明了一种特殊催化剂,可以使水变为汽油 C. 有关部门利用明矾对饮用水进行消毒杀菌,从而解决了灾民饮水难的问题 D. 科研机构发明了一种用植物秸秆生产乙醇的新工艺 18.用括号中的试剂除去物质中所含杂质,所用药品错误的是…………………… ( ) A. CO2中有少量HCl(饱和碳酸氢钠溶液) B. CO中有少量CO2(灼热的氧化铜) C. H2中有少量水蒸气(浓硫酸) D. N2中有少量O2(灼热的铜网) 19.某电镀厂排出的酸性污水中,含有有毒的Cu2+,欲除去Cu2+并降低污水的酸性,可加入 ( ) A. 食盐 B. 生石灰 C. 氧化铁 D. 氢氧化钡 20.科学家发明了一种“碳纳米管温度计”,这种温度计被认定为世界上最小的温度计。研究人员在长约10-6m,直径为10-7m的碳纳米管中充人液态的金属镓。当温度升高时,管中的镓就会膨胀,通过电子显微镜就能读取温度值。这种温度计测量的范围为18℃~490℃,精确度较高,所以它可用于检查电子线路是否异常,测定毛细血管的温度等许多方面。根据以上信息判断下列推测中错误的是……………………… ( ) A. 碳纳米管的体积在10℃至500℃之间随温度变化很小,可忽略不计 B. 金属镓的熔点很低,沸点很高 C. 金属镓的体积在10℃至500℃之间随温度变化比较均匀 D. 金属镓的体积在10℃至500℃之间随温度变化很小,可忽略不计 21.下列说法正确的是………………………………………………………………… ( ) A. HF的命名是氟酸 B. 氧化物中一定有一种元素不是氧元素 C. 含有氢氧根的化合物一定是碱 D. 有盐和水生成的反应一定是中和反应 22.室温下,在pH=1的溶液中可能大量共存的是……………………………… ( ) A. K+、Cl-、SO42-、OH- B. Na+、SO42-、NO3-、CO32-  C. NH4+、Cl-、NO3-、SO42- D. Ba2+、NO3-、Cl-、SO42- C. NH4+、Cl-、NO3-、SO42- D. Ba2+、NO3-、Cl-、SO42-23.如图所示,在一只盛有氢氧化钡溶液的烧杯中,漂浮着一个小塑料块,若小心地向烧杯中滴加与氢氧化钡溶液密度相同的稀硫酸,小塑料块浸入液体中的体积与所加硫酸的体积的关系曲线为 ( ) 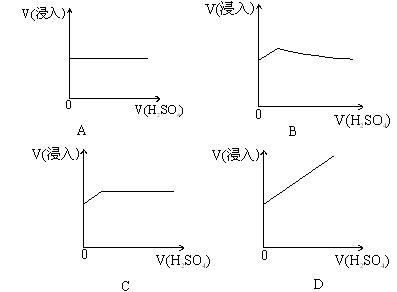 24.向4支装有质量和质量分数均相同的稀硫酸的试管中,分别加入适量的Mg、MgO、Mg(OH)2、MgCO3,反应完全后(反应物均完全反应),对应得到①②③④四个溶液,则其中浓度最大的是… ( ) A. ① B. ② C. ③ D. ④ 25.某同学用一定量的铁与足量稀硫酸及足量氧化铜制单质铜,他设计了以下两种方案: ① CuO 他若按实验原则进行操作,则两者制得单质铜的量为……………………………… ( ) A. ①多 B. ②多 C. 一样多 D. 无法判断 26.从中药麻黄中提取麻黄素可作为平喘药使用,为确定麻黄素的分子式(已知它是由碳、氢、氮和氧四种元素组成的),把10 g麻黄素完全燃烧可得26.67 g CO2和8.18 g H2O,同时测得麻黄素中含氮8.48%,由此可推得麻黄素的分子式为……………………… ( ) A. C20H30NO B. C20H30N2O C. C10H15NO D. C10H15N2O5 27.为研究某一镁铝合金的成分,进行甲、乙、丙三组实验。三组各取30 mL同浓度的盐酸溶液,加入该种镁铝合金粉末。每组实验加入合金质量和产生气体质量的有关数据如下:
根据表中的数据可判断………………………………………………………………… ( ) A. 甲组盐酸不足量 B. 乙组盐酸不足量 C. 丙组盐酸不足量 D. 甲、乙、丙三组均盐酸过量 28.某组成为CaHbNc(a、b、c为正整数)的ABS工程树脂可通过下面的反应制得: C3H3N + C4H6 + C8H8 丙烯腈 1,3-丁二烯 苯乙烯 ABS 则参加反应的原料中丙烯腈和1,3-丁二烯的分子个数之比为……………………( ) A. 29.25℃时,在a g b%的X(OH)2溶液中加入c g XO(X为金属元素其相对原子质量为M),保持温度不变,充分搅拌后仍有溶液剩余,同时有d g X(OH)2沉淀,此时X(OH)2的溶解度为………… ( ) A. 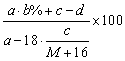 g/100 g H2O g/100 g H2OB. 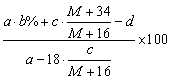 g/100 g H2O g/100 g H2OC. 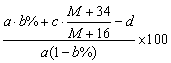 g/100 g H2O g/100 g H2OD. 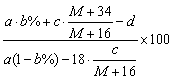 g/100 g H2O g/100 g H2O30.多硫化钠Na2Sx(x>2)在酸性溶液中生成一种臭鸡蛋味的气体和浅黄色沉淀: Na2Sx+2HCl→2NaCl+H2S↑+(x-1)S↓ 向a g Na2Sx加入过量盐酸可得0.672a g沉淀,则x的值是………………………( ) A. 6 B. 5 C. 4 D. 3 31.氧化铜与氢气反应后得到的Cu中常常混有少量Cu2O。Cu2O与硫酸反应的化学方程式为:Cu2O+H2SO4→CuSO4+Cu+H2O。现将5 g Cu与Cu2O的混合物放入足量的稀硫酸中充分反应,过滤得到4.8 g固体,则原混合物中含单质铜的质量为…………………… ( ) A. 4.8 g B. 4.72 g C. 4.64 g D. 4.6 g 32.某混合物由Na2SO4和Na2SO3组成,已知其中氧元素的质量分数为40%,则钠元素的质量分数为……………………………………………………………………………… ( ) A. 24.62% B. 25.09% C. 35.38% D. 无法确定 33.用同一浓度的稀盐酸分别溶解相同质量的CuO和Fe2O3,当两种氧化物都恰好完全反应时,消耗的稀盐酸的体积比为………………………………………………………… ( ) A. 1:2 B. 2:1 C. 2:3 D. 3:2 34.在配置10%的氯化钠溶液的过程中,会导致溶液中氯化钠的质量分数大于10%的原因是……( ) A. 称量氯化钠固体时所用天平的砝码上粘有杂质 B. 将称量好的氯化钠固体倒入烧杯中时,有部分氯化钠固体散落在实验桌上 C. 用量筒量取水时仰视读数 D. 盛装溶液的试剂瓶中有一块碎玻璃 35.50 g镁、锌、铁的混合物与足量的稀硫酸反应,将混合溶液蒸干后可得不含结晶水的固体146 g,则反应生成氢气的质量为……………………………( ) A. 1 g B. 2 g C. 3 g D. 4 g 二、多项选择题(共30分;每小题有1个或2个正确答案;只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给1分,选错一个该小题不给分) 36.下列液体在敞口的容器中放置一段时间后,浓度会降低的是………………… ( ) A. 浓硫酸 B. 浓盐酸 C. 氯化钠溶液 D. 硝酸钾溶液 37.用I2O5可以测定空气受CO污染的程度,发生反应的化学方程式为: I2O5+5CO→I2+5CO2 关于这个反应,下列说法中错误的是………………………………………………… ( ) A. I2O5是氧化剂 B. CO具有还原性 C. I2是还原产物,仅具有还原性 D. 该反应属置换反应 38.下列实验操作错误的是…………………………………………………………… ( ) A. 稀释浓硫酸时,将浓硫酸沿容器壁慢慢倒入水中并搅拌 B. 向烧杯中滴加液体时,滴管不能接触烧杯内壁 C. 为加快固体在水中的溶解,用温度计轻轻地进行搅拌 D. 为防止液体加热沸腾后冲出试管伤人,用橡皮塞塞紧试管后再加热 39.下列各选项中的三种固体通过分别加水就能加以鉴别的是………………………… ( ) A. 氯化钠、硝酸铵、氢氧化钠 B. 氯化钠、硫酸钠、硫酸钡 C. 氢氧化钠、氢氧化钾、氢氧化钡 D. 氯化钠、硫酸钡、无水硫酸铜 40.如图,实验桌上放置的两容器中盛有等体积的乙酸和水两种液体。几天后,两者的体积都明显减少,且乙酸比水减少得多。由此现象得出的正确结论是………………… ( )  A. 乙酸与水都能挥发 A. 乙酸与水都能挥发B. 乙酸比水易挥发 C. 乙酸的熔点比水低 D. 乙酸的沸点比水高 41.现有质量分数为5%的KNO3溶液50 g,要使其溶质的质量分数达到20%,可采用的方法是 ……………………………………………………………………………………… ( ) A. 加入7.5 g KNO3固体 B. 加入9.375 g KNO3固体 C. 蒸发掉40 g水 D. 蒸发掉37.5 g水 42.有一包不纯的Na2CO3样品,其中只含一种杂质,现取该样品5.3 g与足量稀盐酸反应生成2.4 g CO2,则所混杂质可能是………………………………………………… ( ) A. BaCO3 B. K2CO3 C. CaCO3 D. MgCO3 43.有一种化工原料的生产过程是:(a)以煤为燃料煅烧石灰石;(b)用饱和NaCl溶液充分吸收NH3和CO2,析出NaHCO3沉淀,然后煅烧碳酸氢钠;(c)将步骤(a)产生的CaO与H2O反应;(d)消石灰与步骤(b)中的滤液反应,产生氨。该生产过程中涉及的物质(除煤和水外)有:①氯化钠;②氨;③二氧化碳;④氯化铵;⑤消石灰;⑥石灰石;⑦生石灰;⑧碳酸钠;⑨碳酸氢钠;⑩氯化钙。下列叙述正确的是……………… ( ) A. 起始原料是①⑥ B. 起始原料是⑥⑨ C. 最终产品是⑧⑩ D. 最终产品是⑤⑧ 44.某一溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液四种物质中的一种或几种混合形成,现向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图所示。则下列判断正确的是…………………( )  A. 该混合液至少含有硫酸或盐酸中的一种,也可能两种同时含有 B. 该混合液中不可能含有碳酸钠 C. 该混合液中是否含有氯化铜不能确定 D. 从上述信息可知该混合液的组成只可能有一种情况 45.乙醇汽油是由乙醇(C2H6O)与汽油(主要成分可表示为CnH2n+2,n=5~11)按1:9的比例混合而成,它的使用可有效地降低汽车尾气排放。下列有关说法正确的是……………… ( ) A. 相同质量的乙醇和汽油分别完全燃烧,乙醇需要消耗的氧气较多 B. 相同质量的乙醇和汽油分别完全燃烧,汽油需要消耗的氧气较多 C. 乙醇比汽油更易充分燃烧 D. 汽油比乙醇更易充分燃烧 2008年上海市初三化学竞赛(天原杯)预赛试卷 参考答案及评分标准 一、单项选择题(共70分;每小题只有1个正确答案)
二、多项选择题(共30分;每小题有1个或2个正确答案;只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给1分,选错一个该小题不给分)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
