|
第九单元 溶液 素质训练与检测 课题1 溶液的形成 双基落实 1.下列物质中,属于纯净物的是( ) A.豆浆 B.酒精 C.食醋 D.牛奶 2.下列物质中,不属于溶液的是( ) A.啤酒 B.矿泉水 C.汽水 D.液氧 3.溶解适量的固体碘制成消毒液,应该使用( ) A.蒸馏水 B.医用酒精 C.汽油 D.生理盐水 4.下列各组物质充分混合后,能得到溶液的是( ) A.氧化铁加入水中 B.汽油加入水中 C.硫酸铜加入水中 D.花生油加入水中 5.下列各组物质充分混合后,能得到乳浊液的是( ) A.碳酸钙加入水中 B.碘加入水中 C.酒精加入水中 D.植物油加入水中 6.在水中加入高锰酸钾晶体,充分振荡,得到 色的溶液,其中的溶质是 ,溶剂是 。 7.把碘加入酒精中,得到的溶液中的溶质是 ,溶剂是 ,这种溶液叫 溶液,常用作 液。 8.分别将NaCl、NH4NO3、NaOH固体加入到水中,使它们充分溶解,使溶液温度明显升高的是 ,明显降低的是 。 能力提升 1.下列物质中,不属于溶液的是( ) A.自来水 B.葡萄糖注射液 C.液态空气 D.蒸馏水 2.下列叙述中,正确的是( ) A.矿泉水是溶液 B.无色透明的液体属于溶液 C.最常用的溶剂是水 D.酒精只能溶解碘 3.下列“水”中,属于纯净物的是( ) A. 清纯的井水 B.淡化的海水 C.净化的河水 D.实验室配制试剂用的水 4,将二氧化碳通入足量的下列液体中,不能得到溶液的是( ) A.蒸馏水 B.澄清石灰水 C.氢氧化钠溶液 D.汽水 5.把熟石灰加入水中,得到的溶液中的溶质是 ,溶剂是 ,这种溶液叫 溶液,俗称 ,常用于检验 气体。 6.一定量的锌跟一定量的稀硫酸恰好完全反应,所形成的溶液中,溶质是 ,溶剂是 。 7.吃饭时,不小心新衣服上沾上了油污,你有什么办法清除掉油污,使衣服依旧亮丽如新? 拓展创新 1.下列气体通入水中,能得到溶液的是( ) A.二氧化碳 B.氮气 C.一氧化碳 D.甲烷 2.锌粒投入硫酸铜溶液中,充分反应后,锌粒有剩余,所得溶液中的溶质是( ) A.锌 B.硫酸 C.硫酸锌 D.硫酸铜 3.铁和足量稀硫酸充分反应后,所得溶液中的溶质是( ) A.只有硫酸亚铁 B.只有铁 C. 只有硫酸铁 D.有硫酸亚铁和硫酸 4.下列物质投入足量的稀盐酸中,充分振荡。能得到溶液的是( ) A.木炭粉 B.铜粉 C.大理石粉 D.银粉 5.液态空气也是一种溶液,其中的溶剂是 ,主要的溶质是 。 6.在汽油中加入食盐,充分振荡后,得到的是 液;汽油中加入植物油,充分振荡后,得到的是 液。 7.在蔗糖水中,溶质的小微粒是 ,在碘酒中,溶质的小微粒是 ,在食盐水中,溶质的小微粒是 。 8.请设计一个简单的实验,说明矿泉水是溶液,蒸馏水是纯水。
课题2 溶解度 双基落实 1.测定20 ℃时硝酸钾在水中的溶解度时,所用的溶液一定是20 ℃时硝酸钾的( ) A.浓溶液 B.稀溶液 C.饱和溶液 D.不饱和溶液 2.把室温下的不饱和食盐水变成饱和溶液,最好的方法是( ) A.蒸发水 B.加食盐 C.给溶液降温 D.给溶液升温 3.20 ℃时,食盐的溶解度是36 g,它的含义是( ) A.20 ℃时,136 g饱和食盐水中含有36 g食盐 B.在100 g水中最多溶解36 g食盐 C.20 ℃时,饱和食盐水中含有36 g食盐 D.20 ℃时,100 g饱和食盐水中含有36 g食盐 4.下列物质中,当温度升高时,其在水中的溶解度降低的是( ) A.Ca(OH)2 B.KNO3 C.NaCl D.NH4NO3 5.在某温度下的硝酸钾饱和溶液中加入一定量的硝酸钾晶体,溶液中硝酸钾的质量将会( ) A.变大 B.变小 C.不变 D.无法判断 6.在一定的温度下,检验某溶液是否为饱和溶液,最简单的方法是 。 7.在通常情况下,采取 和 的方法,可将不饱和溶液转化为饱和溶液。将一定温度下的饱和食盐水变成不饱和食盐水,最好的方法是 ,将一定温度下的硝酸钾不饱和溶液变成饱和溶液,最好的方法是 。 8.硝酸铵在 10 ℃时的溶解度为 140 g,这说明在 10℃时,将 140 g硝酸铵溶解在 g水中,就可以得到 g硝酸铵饱和溶液。 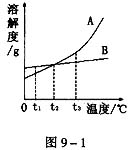 9.根据右图溶解度曲线填写: 9.根据右图溶解度曲线填写:
10.气体的溶解度一般随着温度的升高 ,当温度不变时,随着压强的增大,气体的溶解度 。 能力提升 1.下列叙述中,正确的是( ) A.升高温度时,饱和溶液一定变成不饱和溶液 B.降低温度时,不饱和食盐水可能变成饱和食盐水 C.有晶体析出的溶液一定是浓溶液 D.用加热蒸发的方法,能使医用酒精变成无水酒精 2.在20 ℃时,测得50 g水中溶解18 g氯化钠恰好形成饱和溶液,从实验中可知( ) A.氯化钠的溶解度为 18 g B.氯化钠的溶解度为 36 g C.20 ℃时氯化钠的溶解度为 18 g D.20 ℃时氯化钠的溶解度为36 g 3.某温度下,将5 g氯化钠放入1 10g水中,得到 13.6 g氯化钠溶液,该溶液一定是( ) A.饱和溶液 B.不饱和溶液 C.稀溶液 D.无法判断 4.t ℃时某物质的溶解度 100 g,该温度下,此物质的饱和溶液中下列质量关系正确的是( ) A.溶质:溶液=1:1 B. 溶质:溶剂=1:1 C.溶剂:溶液=1:1 D.饱和溶液的质量一定为200 g 5.某温度下,将 3 g A物质放入7 g水中,得到 10 g溶液,该溶液是( ) A.饱和溶液 B.不饱和溶液 C.浓溶液 D.无法确定 6.20 ℃时,硝酸钾的溶解度是31.6 g,则 20 ℃时,50 g水中最多能溶解 g硝酸钾。 7.20 ℃时,25 g水中最多能溶解9 g食盐,此温度下食盐的溶解度为 。 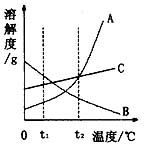 8.右图是A、B、C三种物质的溶解度曲线,请回答:(1)在t1 ℃时,A、B、C三种物质的溶解度由大到小的顺序为 ; 8.右图是A、B、C三种物质的溶解度曲线,请回答:(1)在t1 ℃时,A、B、C三种物质的溶解度由大到小的顺序为 ;(2)在t2 ℃时,用质量相同的 A、B、C三种物质分别配制饱和溶液,所得饱和溶液质量最大的是 ; (3)当A物质中混有少量B、C两种物质时,采用 的方法可以除去它们。 9.在0 ℃时,氮气的溶解度为0.024,这是指在 O ℃和压强为1.01×105 Pa时,1 L水里最多能溶解氮气 。 拓展创新 1.压强增大时,其在水中的溶解度不受影响的是( ) A.NH3 B.SO2 C. CO2 D.KCl 2.将1 g某物质在室温时溶于20 g水中即达饱和,则一般把这种物质划分为( ) A.易溶物质 B.可溶物质 C.微溶物质 D.难溶物质 3.20 ℃时,10 g甲物质可制成30 g饱和溶液,20 g乙物质可制成50 g饱和溶液,则20 ℃时甲与乙的溶解度相比是( ) A. 甲>乙 B.乙>甲 C.甲=乙 D.无法比较 4.已知X物质与Y物质的溶解度都随温度的升高而增大,20 ℃时,10 g水中最多溶解4 g X物质,30 ℃时,20 g水中最多溶解 8 g Y物质,则20 ℃时X与Y的溶解度相比是( ) A.X=Y B.X<Y C.X>Y D.无法比较 5.室温下,把20 g固体A投入80 g水中充分溶解,所得溶液的质量可能是 ,原因是 。  6.在 20 ℃时,将一定量 A的不饱和溶液蒸发10 g水或加入 2 g A,都能得到A的饱和溶液,则20 ℃时,A的溶解度为 。 6.在 20 ℃时,将一定量 A的不饱和溶液蒸发10 g水或加入 2 g A,都能得到A的饱和溶液,则20 ℃时,A的溶解度为 。7.在一个温度不变的密闭容器内,放入一杯饱和的硫酸铜溶液,用细线吊住一块有缺口的硫酸铜晶体浸在溶液中(如右图)过几天后观察到:晶体上的缺口 (填“有”或“没有”)了;晶体的质量 (填“减小”、“增大”或“没变”);此时的硫酸铜溶液是 (填“饱和”或“不饱和”溶液)。 8.右图为某气体的溶解度曲线,根据图中所示,影响气体溶解度的因素有 ;请说明理由(根据图示举例回答)。 9.我国青藏高原有许多盐碱湖,湖水中溶有大量的食盐和纯碱(纯碱的溶解度受温度影响较大),因此那里的农民冬天捞碱,夏天晒盐。请用你学过的知识说明其中的道理。 课题3 溶质的质量分数 双基落实 1.溶质的质量分数为10%的氢氧化钠溶液,对其意义理解不正确的是( ) A.100 g水中溶解有10 g氢氧化钠 B.10 g溶液中含有1 g氢氧化钠 C.溶液中溶质质量与溶剂质量的比为1:9 D.把5 g氢氧化钠固体溶解在45 g水中,可制成 10%的氢氧化钠溶液 2.从100 mL溶质的质量分数为 10%的硫酸溶液中倒出 20 mL,剩下的溶液中溶质的质量分数( ) A.8% B.10% C.12.5% D.80% 3.用400 g溶质的质量分数为20%的氢氧化钠溶液,配制成溶质的质量分数为10%的氢氧化钠溶液,需要加入水的质量是( ) A.100 g B.200 g C.400 g D.800 g 4.把 10 g溶质的质量分数为 20%的食盐水加水稀释到 100 g,则所得溶液中溶质的质量( ) A.增大9倍 B.减小10倍 C.增大10倍 D.不变 5.把5 g食盐溶解在 120 g水中,所得溶液中溶质的质量分数为( ) A.4% B.4.2% C.4.4% D.5% 6.配制一定溶质质量分数的溶液,正确的操作步骤是( ) A.称量(量取)、计算、溶解 B.计算、称量(量取)、溶解 C.计算、溶解、称量(量取) D.溶解、计算、称量(量取) 7.配制溶质质量分数为0.8%的生理盐水 55 g,需要医用氯化钠 g。 8.若配制溶质的质量分数为15%的氯化钾溶液,需要在68 g水中加入 g氯化钾。 9.在实验室配制溶质的质量分数为 10%的氯化钠溶液 100 g,经计算,在 上称量 g氯化钠并倒入干燥洁净的烧杯里,然后用 量取 mL蒸馏水倒入装有氯化钠的烧杯里,并用 不断搅拌,使氯化钠完全溶解,即得所需的溶液。 10.通常的食醋中约合3%~5%的乙酸,计算500 g溶质的质量分数为4%的食醋中,含有乙酸多少克? 11.实验室用石灰石与稀盐酸反应制取二氧化碳。若要制取4.4 g二氧化碳,需要溶质的质量分数为10%的盐酸多少克? 能力提升 1.一定温度下,蒸发某溶液至有少量晶体析出时,保持不变的是( ) A.溶液的质量 B.溶质的质量 C.溶质的溶解度 D.溶质的质量分数 2.在t ℃时,把A物质5 g放入97 g水中充分搅拌,得到 100 g溶液,则溶液中溶质的质量分数为( ) A.3% B.5% C.5.15% D.49% 3.20 ℃时氯化钠的溶解度为36 g,20 ℃时,将20 g氯化钠放入50 g水中充分溶解,所得溶液中溶质的质量分数为( ) A.20% B.26.5% C.36% D.4O% 4.现有100 g溶质的质量分数为 10%的硝酸钾溶液,若要使溶液中溶质的质量分数增大一倍,可采用的方法是( ) A.加入 10 g硝酸钾 B.加入20 g硝酸钾 C.蒸发45 g水 D.蒸发50 g水 5.用硝酸钾晶体配制溶质质量分数为 10%的硝酸钾溶液 100 g,量取蒸馏水的正确操作是( ) A.用 10 mL的量简量取9次 B.用 50 mL的量筒量取2次 C.用 100 mL的量简量取1次 D.用 250 mL的量简量取1次 6.一定温度下,向一定量的不饱和食盐水中加入食盐并充分搅拌,用纵坐标表示溶液中食盐的质量分数(a%),用横坐标表示实验进行的时间(t),其中正确的是( )  7.在 100 g溶质的质量分数为5%的食盐溶液中加入5 g食盐再加100 g水,完全溶解后,溶液的质量为 ,溶质的质量为 ,溶剂的质量为 ,溶质的质量分数为 。 8.工人师傅要用98%的浓硫酸(密度为1.84 g/cm3)稀释成15%的稀硫酸来清洗钢铁的铁锈(水的密度为1 g/cm3),求: (l)55 500mL溶质质量分数为 98%的浓硫酸的质量为 g,其中溶质的质量为 g。 (2)将500 mL 98%的浓硫酸稀释成 15%的稀硫酸,约需用水 mL。 9.将25 g石灰石(主要成份是 CaCO3)放入73 g稀盐酸中(石灰石中的杂质不跟盐酸反应,也不溶于水)恰好完全反应,生成8.8 g二氧化碳气体。试求: (1)石灰石中碳酸钙的质量分数; (2)稀盐酸中溶质的质量分数; (3)反应后溶液中溶质的质量分数。 创新拓展 要配制 50 g溶质的质量分数为 20%的硝酸钾溶液,现提供25 g溶质的质量分数为40%的硝酸钾溶液、20 g溶质的质量分数为15%的硝酸钾溶液及足够多的硝酸钾晶体和蒸馏水,请选用上述的药品,设计三种配制方案填入下表:
单元综合检测A 一、选择题(每小题只有一个选项符合题意) 1.下列物质中,属于纯净物的是( ) A.生理盐水 B.医用酒精 C.“84”消毒液 D.过氧乙酸 2.下列物质中,属于溶液的是( ) A.牛奶 B.碘酒 C.蒸馏水 D.豆浆 3.下列各组物质充分混合后,不能得到溶液的是( ) A.蔗糖加入水中 B.食盐加入植物油中 C.铁粉加入盐酸中 D.植物油加入汽油中 4.澄清的石灰水中,溶质是( ) A.石灰 B.石灰石 C.氧化钙 D.氢氧化钙 5.在一定温度下,某物质的饱和溶液一定是( ) A.浓溶液 B.不能再溶解任何物质的溶液 C.稀溶液 D.不能再溶解该物质的溶液 6.欲将某温度下的一杯饱和的硝酸钾溶液变成不饱和溶液,可采取的方法是( ) A.加热 B.降温 C.加硝酸钾固体 D.加该温度下的硝酸钾饱和溶液 7.下列条件下,二氧化碳在水中溶解度最大的是( ) A. 1×101 kPa、20 ℃ B. 2×101 kPa、10 ℃ C. 2×101 kPa、20 ℃ D. 1×101 kPa、10 ℃ 8.把60 ℃时的硝酸钾饱和溶液冷却到20 ℃时,不发生改变的是( ) A.溶液的质量 B.溶质的质量分数 C.溶剂的质量 D.溶质的溶解度 9.在某温度下的硝酸钾饱和溶液中加入一定量的硝酸钾晶体,溶液中硝酸钾的质量分数将会( ) A.变大 B.变小 C.不变 D.无法判断 10.把 10 g氯化钠的固体放入50 g水中完全溶解后,溶液中散化钠的质量分数为( ) A.10% B.16.7% C.20% D.25% 二、填空题 11.水中加入几滴花生油,充分振荡后,得到的是 液,澄清的石灰水中通入少量的二氧化碳,得到的是 液。 12.将二氧化碳溶于水中,所得溶液中的溶质是 ,加热该溶液,溶质的质量分数会 (填“变大”、“变小”或“不变”)。  13.右图是 A、B、C三种物质的溶解度曲线,回答下列问题: 13.右图是 A、B、C三种物质的溶解度曲线,回答下列问题:(1)A物质在t3 ℃时溶解度为 。 (2)P点表示 。 (3)t1 ℃时,三种物质溶解度由大到小的顺序是 。 (4)要从A物质的饱和溶液中得到A物质,可用的方法是 ,要从 B物质 的饱和溶液中得到B物质,可用的方法是 。 (5)如果A物质中混有少量B物质和C物质,可用 的方法得到较纯的A物质。 三、实验题 14.下列A~F的8种仪器中: 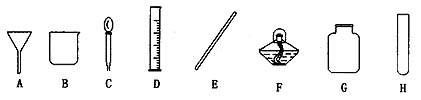 (1)各仪器的名称是:A B C D E F G H ; (2)配制一定质量分数的溶液时要用到的仪器是 (写序号)。 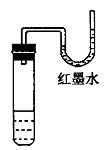 15.将等质量的NaCl、KNO3、NH4NO3、NaOH等4种固体放入试管中,再加入等质量的水,盖好橡胶塞,振荡、静置,观察到的现象如右图所示。则试管中加入的固体是 ,理由是 。 15.将等质量的NaCl、KNO3、NH4NO3、NaOH等4种固体放入试管中,再加入等质量的水,盖好橡胶塞,振荡、静置,观察到的现象如右图所示。则试管中加入的固体是 ,理由是 。四、计算题 16.为了预防“非典”,人们用过氧乙酸(CH3COOH)对家庭居室和公共场所进行消毒。过氧乙酸具有强的腐蚀性和氧化性,使用时一定要稀释。一般家庭用的是溶质质量分数为0.2%~0.5%的过氧乙酸消毒液,现要配制1 L溶质质量分数为0.5%的过氧乙酸消毒液(密度约为l g/cm3),需要溶质质量分数为20%过氧乙酸溶液多少克? 17.将 100 g稀盐酸与足量的铁粉反应,生成氢气0.4 g,求: (1)消耗铁粉的质量; (2)稀盐酸中溶质的质量分数; (3)反应后所得溶液中溶质的质量分数。 单元综合检测B 一、选择题(每小题只有一选项符合题意) 1.下列因素中,与物质在水中溶解度的大小无关的是( ) A.温度 B.溶质的性质 C.压强 D.水的质量 2.下列叙述中,正确的是( ) A.降低温度时,溶液中一定有晶体析出 B.升高温度时,饱和的石灰水变成了不饱和溶液 C.有晶体析出的溶液一定是该温度下的饱和溶液 D.用加热蒸发的方法,能使稀的碳酸溶液变成较浓的碳酸溶液 3.某温度下,a g硝酸钾放入到b g水中,得到硝酸钾溶液的质量(m)是( ) A.m=(a+b)g B.m>(a+b)g C.m<(a+b)g D.A与C可能,B不可能 4.把 1 mL溶质的质量分数为 98%的浓硫酸慢慢注入 4 mL水中配成稀硫酸,若浓硫酸的密度为1.84 g/cm3,则所得稀硫酸中溶质的质量分数为( ) A.36.l% B.31.l% C.30.9% D.19.6% 5.从溶质的质量分数为20%的某溶液中,倒出其体积的3/4后,再加水至原来的体积,然后在倒出其体积的2/3,最后剩余溶液中溶质的质量分数为( ) A.3% B.4% C.5% D.6% 6.现有 100 g溶质的质量分数为 8%的硝酸钾溶液,若要使溶液中溶质的质量分数增大一倍,可采用的方法是( ) A.加入9.5 g硝酸钾 B.加入8 g硝酸钾 C.蒸发46 g水 D.蒸发42 g水 7.向 10%的氯化钠溶液中加入 10 g氯化钠固体,再加 10 g水,此时溶液中氯化钠的质量分数变为15%,则原10%的氯化钠溶液的质量为( ) A.250 g B.200 g C.140 g D.102 g 8.要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是( ) A.游码没有回到零位就开始称量 B.只在称量食盐的托盘垫上了干净的纸 C.所用烧杯不干燥,有少量水 D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中 9.在一定温度下的饱和食盐水里加入少量的硝酸钾晶体,则( ) ①硝酸钾晶体不溶,②硝酸钾晶体溶解,③溶液中食盐的质量分数不变,④溶液中食盐的质量分数减小,⑤溶液中食盐的质量分数增大。 A.①③ B.②③ C.②④ D.②⑤ 10.把某温度下m g的硝酸钾不饱和溶液恒温蒸发水分,直到有少量晶体析出。在此过程中,溶液中溶质的质量分数(a%)与时间(t)的变化关系,可以用下列曲线表示的是( ) 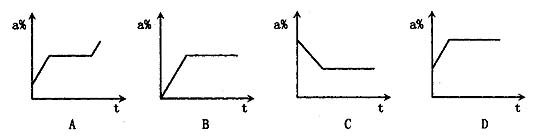 二、填空题 11.一定量的碳酸钙与稀盐酸恰好完全反应,反应后所得的溶液中,溶质是 ,溶 ,溶液的质量 碳酸钙与稀盐酸的质量总和(填“大于”、“等于”或“小于”)。 12.下表是A、B、C、D四种固体各 10 g,在t ℃时完全溶解所需水的最小质量。则t ℃四种固的溶解度(Sx)由大到小的顺序为 。
13.在20 ℃时,取NaCl和Ca(OH)2各 10 g,分别与90 g水充分混合,所得溶液中溶质的质量分数为10%的是 。 14.将 100 g硝酸钾溶液分成量等份,其中一份加入5 g硝酸钾,另一份蒸发掉20 g水,都恰好形成15 ℃时的饱和溶液,则原溶液中硝酸钾的质量分数为 。 15.在t ℃时硝酸钾的溶解度为 a g,该温度下把 b g硝酸钾投入c g水中充分溶解:  三、实验题 16.根据你日常生活的经验,选择身边的物质,用实验探究气体的溶解度与哪些因素有关?请写出实验选用的物质及步骤、现象和结论。 实验选用的物质是 ;
17.如下图所示:在A、B、C. D四个烧杯的水中加入食盐(每勺食盐质量均为5 g),待食盐完全溶解后,所得溶液中溶质的质量分数相等的是 与 (填序号,下同),溶质的质量分数之比为2:1的是 与 。 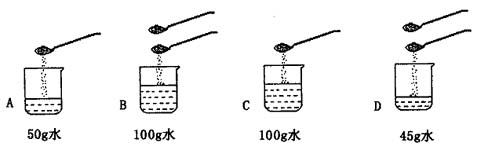 四、计算题 18.一定温度下,将425 g含有A物质的溶液蒸发掉300 g水后,溶液恰好饱和;若另取 85 g原溶液,加入25 g A物质和 40 g水充分搅拌后,溶液也恰好饱和。求饱和溶液中溶质的质量分数是多少? 19.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:
(1)上表中m的数值是 ; (2)反应中矿石有剩余是第 次实验; (3)这种石灰石矿中碳酸钙的质量分数是 ; (4)稀盐酸中溶质的质量分数是 。 自《新课程 新教材 新理念》化学九年级上,本书由北京海淀区教师进修学校编,中国书店出版,地址:北京琉璃厂东街115号,邮编100050。 (责任编辑:admin) |
