“铁与水蒸气的反应装置”的实验效果很不理想。分析原因如下:第一,用酒精喷灯加热,很容易使玻璃管变形,即使是用硬质的石英玻璃管,间隙移动喷灯,玻璃管的软化、变形,甚至破裂的情况很难避免;况且,一经移动,反应速度立刻减慢。
第二,一般说来,只有紧贴在玻璃管壁被加热至红热的铁粉才能跟水蒸气起反应,分散在石棉绒上的其他大量铁粉,由于温度不够高,实际没有发生反应。因此,石棉绒尽管把铁粉分散了,但从效果上看是形同虚设。
第三,烧瓶里产生的大量的水蒸气到了玻璃(反应)管,将会凝聚下来成为液体,这些液体无处可流,只有聚积在高温玻璃管中,十有八九会导致玻璃管破裂。
第四,干燥管在这里更是名不符实。无论用哪种干燥剂所填装的干燥管,总是用以除去仅有的少量水蒸气气体;在本实验条件下,如此大量的水蒸气,无论用哪种干燥剂都起不到预想的干燥效果。
第五,集气试管中有无H2,有多少H2更是心中无数。一句话,教师课堂演示这个实验所承担的风险太大,完全没有绝对成功的把握,需要改进。我们按图1所示进行改进,实验效果好。
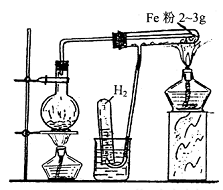
图1
(1)实验成功的关键
①铁粉放在试管底——水蒸气导管的末端;
②烧瓶里仅装20mL~30mL水,先加热烧瓶中的水,待水蒸气把试管加热至发烫,且有少量冷凝水从具支导管流出时,再用酒精灯小心加热试管底部——水蒸气出口与Fe粉相接的地方。
③酒精灯固定加热部位,反应速度一般可以有20mLH2/min,用排水取气法收集在试管里,用以燃烧和做爆鸣实验检验H2。集气时间可以维持15min~20min。
(2)改进后的优点
①不存在水蒸气凝结聚集在被加热的Fe与水蒸气的反应部位,消除了实验的风险。
②排水法收集H2,轻而易举地实现了水蒸气(大量)与H2(少量)的分离,完全可以收集到普通条件下的纯H2。
③装置得到简化,操作的难度降低,实验的成功率明显地提高了。
(责任编辑:admin) |