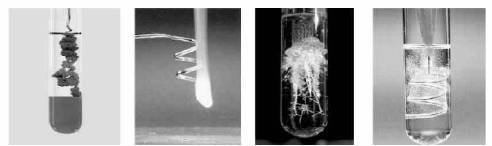
围绕初中化学所学的知识,并结合从这四张彩色照片中所观察到的现象展开讨论,可得出这四张彩色照片分别是:螺旋铝条与CuSO4等铜盐溶液反应形成“铜树”、螺旋镁带在空气或氧气中燃烧、铜丝与AgNO3。溶液反应形成“银根”、螺旋镁带与盐酸等酸溶液反应放出气泡。这四张照片中,第2张照片和第4张照片比较容易判断,第1张照片较难判断,第3张照片最难判断。对于第l张照片学生几乎都说成是螺旋铁条与硫酸铜等铜盐溶液反应,只有在老师的提示下问螺旋铝条与CuSO4溶液反应能不能有此现象发生时,学生才会说有。对于第3张照片,学生很少见到这样的现象,不知从何下手,甚至观察不出反应后生成的溶液为蓝色,这恰好就是解决问题的关键地方。针对第一张“铜树”和第三张“银根”补做两个有趣的实验。
1、有关“铜树”的实验
观察:第1张照片的实验现象是把一根螺旋状的金属条伸入到一种溶液中,该金属条在试管上部分的试液中生成疏松的红色物质,上部分的试液为无色,下部分的试液为蓝色。
分析:下部分的蓝色溶液无金属条,说明下部分的蓝色溶液为原试液,因为金属条未跟蓝色溶液接触,未发生反应。蓝色溶液是含Cu2+的盐溶液,也就是说原试液可以是CuSO4溶液,也可以是CuCl2等溶液,所加入的金属条应该是金属活动顺序表中Cu前面的金属,学生容易想到的是Fe,而教师教学用书上说的却是Al,在试管上部分的无色试液中生成疏松的红色物质就是Cu,反应的化学方程式可能是Fe+CuSO4=FeSO4+Cu,也可能是2Al+3CuSO4=Al2(SO4)3+3Cu。
实验:关于第1张照片到底是铁跟硫酸铜溶液发生的置换反应,还是铝跟硫酸铜溶液发生的置换反应?我们做实验后就会发现第1张照片是铝跟硫酸铜溶液发生的置换反应较为贴切。(下面六张照片从左起的前三张是把螺旋铁条伸入硫酸铜溶液变黑、变红的现象,第4张是放置一天后上部分试液有黄色的现象,第5张是第4张“铜树”的特写,第6张是铝箔绕成的螺旋铝条伸入硫酸铜溶液反应一天后上部分溶液是无色的现象)

因为螺旋状的铁条伸入硫酸铜溶液开始先变黑,一会儿后变为红色,一天后就能形成美丽的“铜树”,但上部分的溶液不是无色,而是黄色,因为生成的硫酸亚铁是有颜色的,时间长后就会被氧化为三价铁离子而使上部分溶液显黄色。对于螺旋状铝条,实验前要先用酸溶液或碱溶液处理其表面,用水清洗后,把其伸入到硫酸铜溶液,一天后就会形成美丽的“铜树”,由于硫酸铝是无色溶液,所以上部溶液是无色的,Al与CuSO4溶液反应生成的红色的“铜树”较为疏松,由于学生未学过盐类水解的知识,不宜解释Al比铁与CuSO4溶液反应生成的红色“铜树”更疏松的原因。
2、有关“银根”的实验
观察:第3张照片的实验现象是把一种不知形状的金属伸入到一种溶液中,生成非常蓬松的白色絮状沉淀,形状为“树根”。尤其是上部的沉淀相对较紧并为黑色。
分析;试液能观察到浅蓝色,说明反应后生成的溶液含Cu,浅蓝色说明生成的Cu浓度小,所以加入的金属应为Cu。这样生成的树根状的、蓬松的白色絮状沉淀就只能是Cu所置换出的Ag,其反应的化学方程式为Cu+2AgNO3=Cu(NO3)2+2Ag
实验;为什么上部的沉淀相对较紧,并为黑色,这种黑色的物质与蓬松的白色絮状沉淀是同一种物质?还是不同的物质?为了回答这个问题,可向学生展示一瓶还原性铁粉,观察其颜色,并补做把一根铜条放入硝酸银溶液中进行反应的实验,可观察到开始铜表面的物质迅速变为黑色,由于此现象非常明显,学生们对此感到很惊讶,过一段时间才会有蓬松的白色絮状沉淀,无色溶液变为浅蓝色,这些现象太能激发起学生的求知探索欲望了。
同样我们可提供铜条和螺旋铜条给学生做实验。
解释:上述做法主要是创设条件,给学生思考问题,提供阶梯,让学生通过思考,恍然大悟,自己说出这种黑色物质和白色沉淀都是Ag。从铁粉是黑色物质的事实说明金属在粉末状时,通常为黑色,而形成整块时为银白色,从而可解释所看到的实验现象是由于开始Cu和AgNO3。溶液反应,生成的触非常少,析出的银粒非常细小为黑色,银粒变大后就会变为白色。生成的沉淀的蓬松和紧密跟什么有关系?跟反应放出的气泡多少和快慢等有关。至于为什么会有气体生成,由于学生目前的知识,暂不讲解。
3、实验注意事项:
(1)螺旋状的铁丝或螺旋状的铜条、螺旋状的铝条的制作,可以用一根铁丝或铜条、铝条绕一支铅笔旋转八、九圈,就可以得到均匀、美观的螺旋状铁丝或铜条、铝条。
(2)为了得到鲜艳亮丽的铜条,必须去除氧化膜,螺旋状的铜条一般因为外表有氧化而没有鲜艳的红色,为了得到鲜艳的红色铜可采用以下方法:
第一种方法是把铜条、螺旋状的铜条放在酒精灯上加热至红,然后迅速伸入装有6ml酒精的试管,反复几次即可得到鲜艳红色的铜,以使铜伸入硝酸银溶液刚反应的那一瞬间现象对比明显。第二种方法是把铜和硝酸银溶液反应后析出的蓬松的“银根”,用水冲洗干净,所得的红色铜同样也是鲜艳亮丽。
(3)为了保证铜和硝酸银溶液反应后,溶液的蓝色要能较深,硝酸银溶液不能太稀。为了使该反应能有多条白色的银根,可以用一根15cm长的导线(要含有多条细小的铜丝的导线)用火烧掉外面的塑料,使一端除去5cm漆包涂层,另一端留下lOcm左右的漆包线。除去漆包涂层的铜丝红色鲜艳,让下一端3cm处的铜丝适当散开,把3cm至5cm处的铜丝旋转拧紧成一股铜丝,加入试管的硝酸银溶液的量从试管底部到液面大约为6cm处,这样可以保证这根铜丝伸入硝酸银溶液里,散开的铜丝下端在离试管底部2cm处悬放,以便生成的白色“银根”能有向下生长的空间,同时拧紧成股的铜丝还能有lcm左右浸入硝酸银溶液里,这样得到的现象非常接近于教科书上的第3张“银根”的照片。
(4)取用硝酸银固体或溶液时,要带橡皮手套以免硝酸银腐蚀手上的皮肤和手指甲,使其变棕黑色。硝酸银很容易腐蚀皮肤和手指甲,需要l到2个星期左右的时间才可能完全褪去。
(责任编辑:admin) |