溶解度曲线中考试题解析
http://www.newdu.com 2025/10/24 06:10:46 普惠英才 佚名 参加讨论
溶解度是初中化学中的一个重要概念,溶解度曲线综合题是近年中考的热点题型。这类题目涵盖面广,综合性强。能较好地考查学生的观察能力、获取信息的能力及知识应用能力。是中考化学的重点,也是学生的失分点。在2011年各地中考化学试题中,出现了许多与溶解度曲线相关的试题,现归纳如下,以供参考。 一、溶解度的意义
解析:由题意知a物质的溶解度随温度的升高而减小,而b物质的溶解度随温度的升高而增大,所以同时符合的图像只有选项C。 答案:C 点评:正确理解溶解度曲线的意义,是解答本题的关键。 三、判断晶体的析出
A.甲物质的溶解度大于乙物质的溶解度 B.甲物质的不饱和溶液温度升高后变成饱和溶液 C.将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体 D.t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有相等质量的溶质 解析:A中没有温度限制,所以不能比较甲、乙溶解度;B中甲的溶解度随着温度的升高而增大,所以甲物质的不饱和溶液温度升高之后,还是不饱和溶液;C因为甲乙两物质的溶解度都随着温度的升高而增大,所以饱和溶液降低温度后都会有晶体析出;D中t2℃时两物质的溶解度相同,所以等质量的饱和溶液中含有相等质量的溶质,但是题中并没有说等质量的饱和溶液,所以错了。 答案:C 点评:该题是一个传统题,历年来考的形式基本相同。 例4 (2011·江苏省南通市)固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线,如图4所示。下列说法错误的是( )
B.t1℃时,物质w在水中的溶解度为mg C.t2℃时,物质W在水中与在乙醇中的溶解度相同 D.将t1℃时物质w的饱和水溶液升温至t2℃有晶体析出 解析:A选项中物质W能溶解在水和乙醇中是正确的;B选项中t1℃时,物质w在水中的溶解度为m g是正确的;C选项中t2℃时,物质W在水中与在乙醇中的溶解度曲线相交,说明t2℃时,物质W在水中与在乙醇中的溶解度相同是正确的;D选项根据溶解度曲线的特点,物质W随着温度的升高溶解度增大,将t1℃时物质w的饱和水溶液升温至t2℃时饱和溶液变成不饱和溶液,没有晶体析出。 答案:D
四、判断饱和溶液和不饱和溶液的转化 例5 (2011·盐城)如图5为A、B、C三种固体物质(不含结晶水)的溶解度曲线。下列说法错误的是( ) A.t1℃时,三种物质中B的溶解度最大 B.t2℃时,取三种物质各a g分别放入100g水中充分溶解,只有C物质能形成饱和溶液 C.将等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,A溶液中析出的晶体质量最大 D.可用增加溶剂的方法使接近饱和的B溶液变为饱和溶液 解析:从溶解度曲线上可以t1℃时三种物质的溶解度B>A=C;t2℃时三种物质的溶解度只有C的溶解度小于ag所以只有C物质能形成饱和溶液;从溶解度曲线上可以看出由t2℃降温到t1℃时,A物质的溶解度变化最大,所以等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,A溶液中析出的晶体质量最大;使接近饱和的B溶液变为饱和溶液可以采用加入溶质B,蒸发溶剂和降低温度的方法。 答案:D 点评:本题结合溶解度曲线考查溶解度、饱和溶液、结晶和饱和溶液与不饱和溶液的相互转化。解答此类题目的关键是结合溶解度曲线认真分析,牢固掌握溶解度的四个方面,深入理解结晶的定义和结晶出的质量与单位饱和溶液质量的关系,特别注意C类物质的饱和溶液转化为饱和溶液时应该采用升高温度。 五、溶解度和溶质质量分数的相关计算
A.甲的溶解度人干乙的溶解度 B.t℃时,甲、乙饱和溶液中溶质的质量分数相等 C.升高温度能使接近饱和的甲溶液变为饱和溶液 D.10℃时,分别用100g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量 解析:溶解度随温度的变化而变化,所以说溶解度时,必须限定温度,所以A不对;甲物质的溶解度随温度的升高而增大,所以C不对;10℃时,甲的溶解度比乙小,分别用100g水配制甲、乙的饱和溶液,所需甲的质量应小于乙的质量。 答案:B 点评:考查了溶解度曲线和溶液的分类、溶质质量分数等问题。
A.A的溶解度都大于B的溶解度 B.t1℃时,用等量水分别制成的A、B饱和溶液中,A的质量比B大 C.t2℃时,A、B两种饱和溶液中,溶质的质量分数相等 D.A、B两种饱和溶液都从t3℃降温到t2℃,析出的晶体一定等量 解析:由溶解度曲线可知,t2℃时,A、B两物质的溶解度相等,所以该温度下,两物质的饱和溶液的溶质质量分数一定相等,故C正确;t1℃时,A的溶解度小于B的溶解度,用等量水分别制成的A、B饱和溶液中,A的质量比B小,故A、B错误;A的溶解度比B受温度影响大,所以等质量的A、B两种饱和溶液从t3℃降温到t2℃,析出晶体的量A一定大于B,故D错误。 答案:C 点评:本题考查溶解度曲线的意义。图中所示的温度,溶解度曲线的趋势、交点是解题的关键。 纵观2011年各地中考试题,有关溶解度曲线的综合题在试题设计上,常将溶解度的概念及意义、结晶的方法、饱和与不饱和溶液的概念及其转化、溶质质量分数及相关计算等核心知识与溶解度曲线结合起来,突出命题的能力立意,这类试题仍将是中考命题的重点。 |
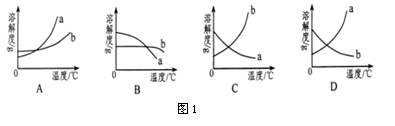 例1 (2011·嘉兴)将a、b两种物质的饱和溶液升高温度后,发现a溶液有晶体析出,b溶液没有明显现象。再向b溶液加入少许b晶体,晶体消失。则图1中能正确表示a、b两物质溶解度曲线的是( )
例1 (2011·嘉兴)将a、b两种物质的饱和溶液升高温度后,发现a溶液有晶体析出,b溶液没有明显现象。再向b溶液加入少许b晶体,晶体消失。则图1中能正确表示a、b两物质溶解度曲线的是( ) 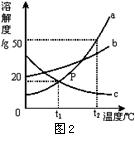 (2)t1℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗? (填“能”或“不能”)。
(2)t1℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗? (填“能”或“不能”)。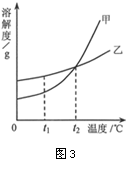 例3 (2011·河北)根据图3所示的溶解度曲线判断,下列说法正确的是( )
例3 (2011·河北)根据图3所示的溶解度曲线判断,下列说法正确的是( )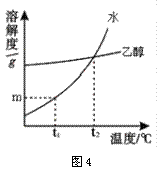 A.物质W能溶解在水和乙醇中
A.物质W能溶解在水和乙醇中 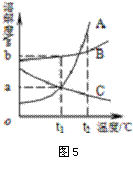 点评:本题主要考查溶解度和溶解度曲线的相关知识,本题的亮点是一种物质溶解在不同的溶剂中,解答本题要明确溶解度概念的“四要素”和溶解度曲线的意义。
点评:本题主要考查溶解度和溶解度曲线的相关知识,本题的亮点是一种物质溶解在不同的溶剂中,解答本题要明确溶解度概念的“四要素”和溶解度曲线的意义。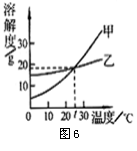 例6 (2011·河南省)如图6是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
例6 (2011·河南省)如图6是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )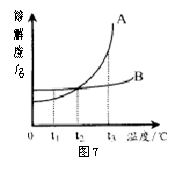 例7 (2011·江苏泰州)如图7是A、B两种固体物质的溶解度曲线,下列说法正确的是( )
例7 (2011·江苏泰州)如图7是A、B两种固体物质的溶解度曲线,下列说法正确的是( )