《酸和碱》“知识点”与“考点”
http://www.newdu.com 2025/11/07 07:11:35 人民教育出版社 佚名 参加讨论
《酸和碱》“知识点”与“考点” 山东省滕州市蒋庄矿区学校 王宪德 本单元用趣味实验和身边常见的物质为载体考查溶液的酸碱性及遇指示剂的变色情况,其中酸、碱的性质和用途是初中化学中的重要知识,是中考试题所占分值较大的一部分内容。同时,通过对土壤、雨水、工业废水等的pH的测定,从而判断这些地方的污染情况是中考的热点试题。继续紧密关注与日常生活、工农业生产实际及学科间知识渗透,注重用实验手段分析理解及获取酸、碱的知识,是今后命题的方向,请同学们多加关注并积累相关资料以备应考。 知识点1 考查酸与碱的概念及识别方法 考查点在于:(1)酸、碱概念辨析。含有H的不一定是酸,如NaHSO4溶液呈酸性(里面含有H+),但NaHSO4属于盐。含有OH的不一定是碱,如Cu2(OH)2CO3属于盐。(2)酸和碱的识别方法:①尝试法(针对生活中常见的食品等而采取的方法);②酸碱指示剂法(需要知道某物质的酸碱性而采用的);③试纸法(蓝色石蕊试纸、红色石蕊试纸、pH试纸等)。 例1 下图表示的是身边一些物质在常温下的近似pH,有关这些物质的比较和判断正确的是 ( ) 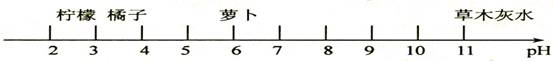 A.柠檬的酸性比橘子弱 B.橘子汁显碱性 C.草木灰水的碱性最强 D.萝卜显中性 思路点拨 溶液的pH越小,其酸性越强,pH越大,其碱性越强。从图示可看出草木灰水的pH=11,溶液呈碱性。答案为C。 知识点2 考查浓酸强碱的物理特性及其用途 考查点在于:(1)浓盐酸和浓硝酸的挥发性(在空气中易形成白雾,导致溶质质量分数都变小)。浓硫酸的吸水性(用作干燥剂,导致溶质质量分数变小)。浓稀硝酸与浓硫酸具有强氧化性(与金属发生的不是置换反应,即得不到氢气而是水)和腐蚀性。(2)固体氢氧化纳、氧化钙、氢氧化钙不能敞口放置的原因(具有吸水性可用作干燥剂)。氢氧化钠溶液、氢氧化钙溶液(俗称石灰水)不能敞口放置的原因(吸收空气中的二氧化碳而变质)。常以物质的名称――俗称――化学式――性质――用途等这条线来考查。 例2 若将浓盐酸和浓硫酸敞口放置在空气中,一段时间后,可以肯定的是 ( ) A.溶质质量都减少 B.溶剂质量都增大 C.溶液质量都增大 D.溶质的质量分数都减小 思路点拨 浓盐酸因挥发出氯化氢气体使溶液的质量减小,导致溶质质量分数变小。浓硫酸因吸水使溶液的质量变大,导致溶质质量分数变小。答案为D。 知识点3 考查酸与碱的化学性质及其用途 考查点在于:(1)酸溶液都电离出H+ ,碱溶液都电离出OH-,决定了它们各有类似的化学性质,而物质的性质决定其用途。例如,酸碱与指示剂的反应可用来检测溶液酸碱性;稀酸与较活泼金属的反应可用来制取氢气(稀硝酸除外),酸碱中和(实质是H++OH-=H2O)可用来治疗人的胃酸过多、中和酸性土壤和工业污水,稀酸与碳酸盐反应可用来制取二氧化碳气体,碱溶液与酸性氧化物的反应可用来解决温室效应、酸雨问题等。(2)Cl-的特征反应(Cl-+Ag+= AgCl↓,该沉淀不溶于稀硝酸);SO42-的特征反应(SO42- +Ba2+ = BaSO4↓,该沉淀不溶于稀硝酸)。 例3 在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应。请与他们一起完成实验方案的设计、实施和评价。 (1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(20℃)。测定某NaOH溶液的pH,pH ______7(选填“大于”、“等于”或“小于”)。将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH,pH 小于7。结论:稀H2SO4与NaOH溶液发生了化学反应,并且_______过量。 (2)方案二:观察______________________________。(根据图示实验步骤,概括方案要点) 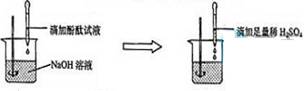 结论:稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为_________________。 结论:稀H2SO4与NaOH溶液发生了化学反应,反应的化学方程式为_________________。(3)上述两个方案在设计思想上的相同点是______________________________________。 (4)为了进一步获取稀H2SO4与NaOH溶液确实发生了化学反应的证据,依据中和反应是___________(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀H2SO4与NaOH溶液进行实验,整个实验中至少需要测定溶液温度_______次。 思路点拨 本题综合考查了酸碱中和测定等的相关知识。(1)原溶液为碱溶液,pH大于7。酸碱反应后,pH 小于7,说明 稀H2SO4过量;(2)根据图示可看出,稀H2SO4加入滴加酚酞试液的NaOH溶液是否有颜色变化,反应的化学方程式为H2SO4+2NaOH=Na2SO4+2H2O;(3)H2SO4与NaOH溶液发生了化学反应;(4)中和反应是放热的,为确保实验的准确性,至少需要测定溶液温度三次。 知识点4 考查酸与碱中有关化学方程式的计算 考查点在于:(1)化学方程式中所表示的反应物和生成物都是指纯净物,遇到不纯物质时,需要将不纯物质换算成纯净物质的质量,计算关系为:纯净物的质量=不纯物的质量×纯净物的质量分数。如果是体积,要根据密度公式转化成质量。(2)对于多步反应的计算(从一个化学反应中求出的质量,用此量再进行另一个化学反应或几个化学反应的连续计算,求最后一个化学反应的量)用关系式法(利用化学反应方程式中的物质间的质量关系列出比例式,通过已知的量来求未知的量)较为简单。注意解题格式。 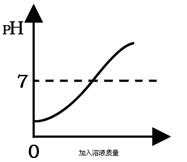 例4 酸与碱作用生成盐和水的反应,叫中和反应。在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示: 例4 酸与碱作用生成盐和水的反应,叫中和反应。在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示:(1)要得到此变化曲线,所进行的操作是 (填序号)。 ①将稀盐酸滴加到氢氧化钠溶液中 ②将氢氧化钠溶液滴加到稀盐酸中 (2)假设实验中使用的酸和碱的密度均以1.0 g/mL计。若测定中取用盐酸溶液25 mL,氢氧化钠溶液中溶质的质量分数为4.5%,当二者完全中和时用了氢氧化钠溶液24.5 mL,试计算盐酸溶液中溶质的质量分数(精确到1%)。 思路点拨 本题将酸碱中和反应的知识与溶液的pH值及其变化联系一起进行考查。(1)据图分析,一开始原溶液的pH<7可推知呈酸性,接着溶液的pH逐渐升高,可推知滴加的是碱溶液,应选②;(2)欲求盐酸溶液中溶质的质量分数,需要求出盐酸溶质的质量(溶液的质量为25 mL×1.0 g/mL=25 g),所以得先把消耗掉的氢氧化钠溶液中溶质的质量求出来:24.5 mL×1.0 g/mL×4.5%=1.10 g,进而根据化学方程式NaOH+HCl=NaCl+H2O,求出盐酸溶液溶质的质量分数约为4%(计算过程略)。 二、中考链接 1.(2011·盐城)柠檬酸(C6H8O7)是一种常用于制汽水、果冻、水果糖的添加剂。柠檬酸属于( ) A.单质 B.氧化物 C.化合物 D.混合物 2.(2011·大连)下表是一些食物的pH,胃酸过多的病人空腹时最宜食用的是 ( )
A.橘子 B.葡萄 C.牛奶 D.玉米粥 3.(2011·苏州)盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质。下列有关叙述正确的是 ( ) A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾 B.稀盐酸和稀硫酸都可用于除铁锈 C.浓盐酸、浓硫酸都可用来干燥氧气 D.在稀盐酸、稀硫酸中滴加氢氧化钡溶液,都有白色沉淀 4.(2011·南昌)下列物质暴露在空气中质量会减轻的是 ( ) A.浓盐酸 B.铁粉 C.生石灰 D.石灰水 5.(2011·滨州)以下推理正确的是 ( ) A.酸中都含有氢元素,所以含有氢元素的化合物一定是酸 B.碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性 C.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 6.(2010·楚雄州)小明同学取下列生活中的物质,测得其pH如下表所示:
由此判断: (1)酸性最强的物质是___________________。 (2)能使无色酚酞试液变红色的物质是_______________________(填一种物质即可)。 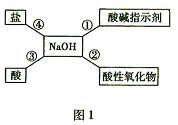 (3)正常雨水的pH约为5.6。小明生活的环境所降的雨水_____(填“属于”或“不属于”)酸雨。 (3)正常雨水的pH约为5.6。小明生活的环境所降的雨水_____(填“属于”或“不属于”)酸雨。7.(2010·重庆綦江)归纳总结是学习化学的重要方法,小明同学用图l总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。 (l)为了验证反应①,小明将无色酚酞试液滴入NaOH液中,溶液变成 色。 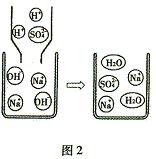 (2)依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为: 。 (2)依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为: 。(3)小明用徽观示意图(图2)来说明反应③的发生,用化学反应方程式表示为: 。 从该图可以看出,反应前后没有发生变化的徽观粒子有 。 (4)为了验证反应④能够发生,你选择的物质是 。 A.Na2CO3 B.HCl C.CuSO4 D.NaCl 8.(2010·陕西)构建知识网络,可以帮助我们理解知识间的内在联系。右图是盐酸与不同类别物质之间反应的知识网络。 (1)图中M应为 类物质。 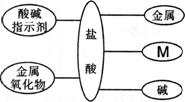 (2)写出一种能与盐酸反应的金属 。 (2)写出一种能与盐酸反应的金属 。(3)盐酸能与碱反应的实质是盐酸中的 (写离子符号)与碱中的OH?反应生成H2O。 (4)用盐酸除铁锈(主要成分Fe2O3)的化学方程式是 。 9.(2011·武汉) 某无色溶液可能由盐酸、氢氧化钠溶液、氯化钠溶液、碳酸钠溶液中的一种或几种混合而成。为探究其组成,小华同学进行了如下实验: Ⅰ、取适量样品放入试管中,滴加酚酞溶液,溶液变成红色。再向试管中逐滴加入过量的氢氧化钙溶液,观察到有沉淀产生。过滤,所得滤液为红色。 (1)由实验Ⅰ中的现象可推断出样品中一定含有的物质是________(写化学式,下同),一定不含有的物质是________; 为了进一步探究样品中可能含有的物质是否存在,小华继续进行了如下实验: Ⅱ、取适量实验Ⅰ所得的红色滤液放入试管中,滴加过量的稀硝酸,溶液变无色。再向试管中逐滴加入适量的硝酸银溶液至恰好完全反应,观察到有白色沉淀生成。过滤,所得滤液为无色。 Ⅲ、从稀硫酸、氢氧化钡溶液、氯化钡溶液、硝酸钾溶液中选择一种试剂,代替实验Ⅰ中的氢氧化钙溶液进行实验,其余的试剂及操作与实验Ⅰ的均相同。 通过实验Ⅱ和实验Ⅲ,小华得出结论:样品中可能含有的物质确实存在。 (2)实验Ⅱ所得无色滤液中,除酚酞以外,还含有的溶质为_____; (3)实验Ⅲ中代替氢氧化钙溶液的试剂是________溶液,可观察到的现象为________。 10.(2010·汕头)某探究小组同学对某工业废水(含有H2SO4、HNO3)中H2SO4的含量进行测定。取50 g废水于烧杯中,加入足量BaCl2溶液,过滤、洗涤、干燥,得BaSO4固体11.65 g。请回答: (1)50 g废水中H2SO4的质量。 (2)若改用KOH溶液来测定50 g废水中H2SO4的含量,结果可能会 (填“偏低”、“偏高”、“不变”),原因是 。 参考答案 1.C 2. D 3.B 4.A 5.B 6.(1)柠檬汁;(2)肥皂水(或洗洁精);(3)属于 7.(1)红;(2)2NaOH +CO2 = Na2CO3 + H2O;(3)2NaOH +H2SO4 = Na2SO4 + 2H2O Na+和SO42-;(4)C 8.(1)盐;(2)Zn或锌(其他合理答案均可);(3)H+;(4)Fe2O3 + 6HCl = 2FeCl3 + 3H2O 9.(1)Na2CO3 HCl;(2)HNO3 NaNO3 Ca(NO3)2;(3)BaCl2 有白色沉淀产生,滤液仍然呈红色 10. 解:(1)设50 g废水中H2SO4的质量为x H2SO4 + BaCl2 = BaSO4↓ + 2HCl 98 233 x 11.65 g 答:50 g废水中H2SO4的质量为4.9 g。 (2)偏高 废水中含有HNO3,会消耗KOH (责任编辑:admin) |
- 上一篇:什么是原盐
- 下一篇:复分解反应及其发生的条件