2018年中考化学考题剖析及压轴题预测(三)
http://www.newdu.com 2025/11/05 12:11:11 三好网 佚名 参加讨论
2018年中考化学考题剖析及压轴题预测(三)。压轴题一般指试卷的最后一道大题,往往是计算题,中考化学的压轴题一般与图像、表格数据分析处理,实验过程图以及标签等有关,考查学生的综合处理能力,今天老师就带大家一起来剖析往年的计算型压轴题并预测今年的压轴题。  【考题剖析】 1.【2017年四川省内江市】一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(其分子式式C15H10N2O2)。请回答下列有关问题; (1)二甲苯烷二异氰酸酯(C15H10N2O2)中氢、氧元素的质量比为______(填最简整数比)。 (2)二甲苯烷二异氰酸酯(C15H10N2O2)的相对分子质量为_______。 (3)500g二甲苯烷二异氰酸酯中含氮元素的质量为____________g. 【答案】(1)5:16;(2)250;(3)56 【解析】(1)二甲苯烷二异氰酸酯(C15H10N2O2)中氢、氧元素的质量比为:1×10:16×2=5:16;(2)二甲苯烷二异氰酸酯(C15H10N2O2)的相对分子质量为:12×15+1×10+14×2+16×2=250;(3)500g二甲苯烷二异氰酸酯中含氮元素的质量为:500g×28/250×100%=56g 【名师点睛】该题考查了物质的化学式的书写(含碳元素的化合物)、化学式表示的意义以及根据化学式进行的简单计算 2.【2017年四川省广安市】一定质量的金属铁和稀硫酸恰好完全反应,产生气体的质量为0.2g。 (1)反应后溶液中溶质FeSO4的质量为_____g。 (2)向反应后的溶液中加入BaCl2溶液,当加入的BaCl2溶液质量为208g时,恰好完全反应,此时生成沉淀的质量为________g。 (3)计算所加BaCl2溶液的溶质质量分数__________。 【答案】(1)15.2。(2)23.3(3)10%  设刚好完全反应时,加入氯化钡的质量为y,生成沉淀质量为m FeSO4 + BaCl2 =BaSO4 ↓+ FeCl2 152 208 233 15.2g y m 152/15.2g =208/y y=20.8g 152/15.2g=233/m m=23.3g 所加BaCl2溶液的溶质质量分数为 20.8g÷208g×100%=10% 答:略 【名师点睛】该题为常规计算题,解题时依据解题步骤及格式进行。 【试题预测】 1.尿素[CO(NH2)2]在工农业生产中应用广泛。 (1)尿素溶液能除去工业废气Cl2,化学方程式为:CO(NH2)2+H2O+3Cl2=N2+CO2+6X,则X的化学式是_________。 (2)尿素是目前使用量较大的一种,_____(选填“氮”“磷”或“钾”)肥,适用于各种植物。某水田施加7.2千克尿素,其中含氮元素多少千克? 【答案】(1)HCl;(2)氮、3.36千克 【解析】(1)据质量守恒定律可知,化学反应前后原子的种类、个数不变,反应前有2个氧原子、1个碳原子、 6个氢原子、2个氮原子、6个氯原子,反应后有2个氧原子、1个碳原子、 2个氮原子,所以一个X的分子中有1个氢原子、1个氯原子;X的化学式为HCl;(2)尿素中含有氮元素,为氮肥; 7.2千克尿素中含氮元素的质量为:7.2千克 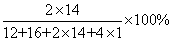 =3.36千克 =3.36千克【预测指数】★★★★ 2.一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(其分子式式C15H10N2O2)。请回答下列有关问题; (1)二甲苯烷二异氰酸酯(C15H10N2O2)中氢、氧元素的质量比为______(填最简整数比)。 (2)二甲苯烷二异氰酸酯(C15H10N2O2)的相对分子质量为_______。 (3)500g二甲苯烷二异氰酸酯中含氮元素的质量为____________g. 【答案】(1)5:16;(2)250;(3)56  【预测指数】★★★★★ 3.某白色粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种。某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量)。 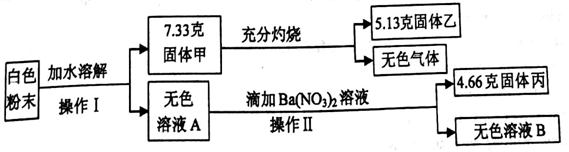 (1)操作I、Ⅱ的名称是______。 (2)无色气体的质量是_____克。 (3)固体甲的成分是______。 (4)这种白色粉末中一定不含有_____。 (5)求白色粉末中肯定含有的物质总质量。 【答案】(1)过滤;(2)2.2;(3)碳酸钙与硫酸钠、硝酸钡;(4)硫酸铜;(5)11.87克 【解析】(1)过滤能将难溶性固体与液体分离;(2)据质量守恒定律可知反应前后物质的总质量不变,所以无色气体的质量是7.33g-5.13g=2.2g;(3)固体溶于水得无色溶液,说明固体中一定不含硫酸铜;能与硝酸钡反应生成沉淀说明有硫酸钠,同时,7.33g固体灼烧后得固体余物5.13g,可判断固体中有硝酸钡,溶于水时生成了硫酸钡沉淀;学科#网 设碳酸钙的质量为x; CaCO3?高温CaO+CO2↑ 100 44 X 2.2g 100/x=44/2.2g x=5g 所以7.33g固体中硫酸钡的质量为2.33g 设生成2.33克硫酸钡沉淀需要硝酸钡的质量为y Na2SO4+Ba(NO3)2 = BaSO4↓+ 2NaNO3 261 233 Y 2.33g 261/y=233/2.33g y=2.61g 生成硫酸钡的总质量为6.99g,则硫酸钠的质量为m Na2SO4+Ba(NO3)2 = BaSO4↓+ 2NaNO3 142 233 m 6.99g 142/m=233/6.99g m=4.26g 固体中一定有的碳酸钙与硫酸钠、硝酸钡的总质量为5g+4.26g+2.61g=11.87g 【预测指数】★★★★ (责任编辑:admin) |