醇的性质
醇分子的羟基可和另外醇分子的羟基相互形成氢键,也可和水形成氢键,所以醇的熔沸点比分子量相同的烃高,低级的醇也易溶于水,多元醇的羟基较多,所以熔沸点更高,更易溶于水,液体的粘度较大。
醇的化学性质主要由羟基官能团决定,键的断裂方式主要有氢氧键断裂和碳氧键断裂方式,具体表现在以下方面:
1.与活泼金属的反应醇可与活泼金属(K、Ca、Mg、Na)反应生成H2,但反应比水慢。
2ROH+2Na→2RONa+H2↑
醇的反应活性:甲醇>伯醇>仲醇>叔醇。醇和钾、钠等金属反应生成的化合物如醇钠,是比NaOH更强的碱。
2.生成卤烷的反应
醇与氢卤醇反应是制卤烷的常用方法之一,不同的氢卤酸反应活性不同,HI、HBr较活泼,与各类醇均可反应。HCl活性较差,与不同类醇的反应难易不一,主要决定于醇的活性。醇的活性如下:3°ROH>2°ROH>1°ROH
⑴卢卡氏试剂无水ZnCl2固体溶于浓盐酸的溶液称卢卡氏试剂,常用于鉴别伯、仲、叔醇。
1°ROH不反应,加热才反应
2°ROH常温,5分钟后反应。
3°ROH1分钟内浑浊
⑵醇与卤代磷、亚硫酰氯(SOCl2)反应也可制得卤烷。
3ROH+PBr3→3RBr+H3PO4
三卤化磷不需先制备,如PBr3、PI3可直接用磷和卤素混和物。
ROH+PCl5→RCl+POCl3+HCl
ROH+SOCl2→RCl+HCl+SO2
上述反应以亚硫酰氯最有实用性,因产物卤代烃为液体,HCl、SO2均以气体形成放出,产物易分离。
3.脱水反应
温度较低时,醇易分子间脱水生成醚,温度较高时,易分子内脱水发生消反应,醇消去时,也服从札依采夫规则。

4.氧化反应
伯醇氧化可得到醛,仲醇氧化生成酮。
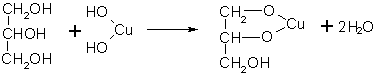
5.多元醇多元醇化学性质与醇相似,但可与新制Cu(OH)2生成绛蓝色溶液。
(责任编辑:admin) |
织梦二维码生成器
------分隔线----------------------------