|
2013年中考化学试题汇编——金属和金属材料(三) 山东省微山县鲁桥一中 黄尊英 51.(2013.遂宁)已调平的托盘天平(高灵敏度)两边各放一个等质量的烧杯,向烧杯中倒入质量相等、质量分数也相等的足量的稀硫酸,然后在左边的烧杯中放入一定质量的铁粉,同时在右边的烧杯中放入等质量的锌粉,在反应过程中天平指针的偏转情况为( ) A. 先左后右 B. 先右后左 C. 不偏转 D. 无法确定 52.(2013.湘潭市)在托盘天平的两边各放一只烧杯,调节天平平衡,向两烧杯中分别注入等质量、等质量分数的稀硫酸(足量),然后向右盘的烧杯中放入一定质量的Fe粉,同时向左盘的烧杯中放入与Fe粉等质量的Zn粉,反应过程中可能出现的现象是 ( ) A.天平最终仍然平衡 B.天平指针先偏向左盘,后偏向右盘 C.天平指针始终偏向右盘 D.天平指针先偏向右盘,后偏向左盘 53.(2013.眉山市)下图是用回收废料来制取铜,同时制取FeSO4·7H2O的流程图。下列说法中不正确的是( ) 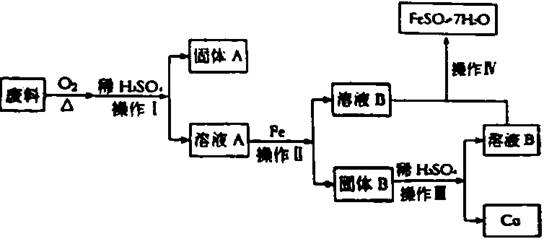 A.操作Ⅰ、Ⅱ、Ⅲ都是过滤 B.操作Ⅳ为蒸发结晶 C.固体B与稀H2SO4反应的化学方程式为:Fe + H2SO4 = FeSO4 + H2↑ D.溶液A与Fe反应的化学方程式为:3CuSO4 + 2Fe = 3Cu + Fe2(SO4)3 54.(2013.滨州)下列现象和事实,可用金属活动性作合理解释的是( ) ①金属镁在空气中比铝更容易燃烧,说明镁比铝的活动性强 ②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强 ③用硫酸铜、石灰水配置农药波尔多液时,不能用铁制容器 ④尽管金属的种类很多,但在自然界中,仅有少数金属(银、铂、金)以单质形式存在. A. ①② B. ①③④ C. ③④ D. ①②③④ 55.(2013.广州市)下列事实不能证明甲的金属活动性比乙强的是( ) A.自然界中甲元素只以化合物形式存在,乙元素有单质形式存在 B.甲能与盐酸反应而乙不能 C.甲能从乙的盐溶液中置换出乙 D.化合物中甲元素显+2价而乙元素显+3价 56.(2013.河北省)把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中。再把X加入到Z (NO3)2溶液中,M加入到YNO3溶液中。反应关系如图2所示。 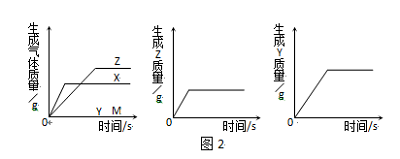 据此判断四种金属的活动性顺序为( ) A.Z>X>M>Y B.X>Z>M>Y C.X>Z>Y>M D.Y>M>Z>X 57.(2013.绍兴市)进行如图实验,加热一段时间后,可观察到有红色物质出现,说明氢气具有( )  A.还原性 B.可燃性 C.氧化性 D.助燃性 58.(2013.南宁市)人类的生活和生产都离不开金属材料。 (1)铁生锈的条件是:铁与空气和__________直接接触。 (2)根据铁生锈的条件,自行车支架采取的防锈措施是_____________________。 (3)某同学为了验证镁、铁、铜的活动性顺序,他选择了打磨过的铁丝,你认为他还需要先的另外两种溶液是____________溶液和______________溶液。请根据选定的试剂写出上述实验中发生反应的一个化学方程式________________________________________。 59.(2013.陕西省)(5分)随着人们生活水平的不断提高,汽车已走进千家万户。制造汽车要用到含铜、铁、铝等成分的多种金属材料。 (1)在汽车电路中,经常用铜作导线,这是利用了铜的 性。 (2)车体多用钢材制造。其表面喷漆不仅美观,而且可有效防止与 接触而生锈。 (3)工业上用CO还原赤铁矿冶炼金属铁的化学方程式为 。 (4)在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是 。(填一种即可) 60.(2013.大连市)钢铁是使用最多的金属材料。 (1)铁制品在一定条件下能生锈,疏松的铁锈不能阻碍里层的铁继续与 ① 反应,因此铁制品可以进一步锈蚀。防止自行车链条生锈的合理措施是 ② 。用盐酸除铁锈的化学方程式为 ③ 。 (2)用一氧化碳和赤铁矿炼铁的化学方程式为 ① 。回收利用废旧金属制品的目的之一是 ② 。 61.(2013.北京市)(6分)铜是人类最早利用的金属之一。 (1)下列铜制品中,利用金属导热性的是 (填字母序号)。  A.铜质奖牌 B.铜导线 C.铜火锅 (2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为 。 (3)利用废旧电池铜帽(含 Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流 程如下(反应条件已略去): 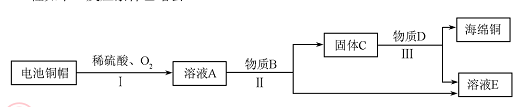 已知: ①过程Ⅱ中分离操作的名称是 。 ②过程Ⅲ中有气体产生,反应的化学方程式为 。 ③A~E 中含铜、锌两种元素的物质有 (填字母序号)。 62.(2013.河南省)(4分)某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。 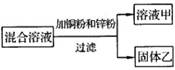 (1)向固体乙上滴加盐酸时 (填“有”或“没有”)气泡产生。 (2)溶液甲中一定含有哪些溶质?(写化学式) (3)请写出该实验过程中所发生反应的化学方程式。 63.(2013.大连市)(5分)取铜、锌混合粉末,在空气中充分灼烧后,加入稀硫酸至固体恰好溶解,再加入一定量的铁粉,充分 (1)滤渣中一定 (2)设计实验方案,探究滤渣成分和与滤渣成分对应的滤液中溶质成分,写出实验操作、预期现象及结论。 64.(2013.绍兴市) 学习了金属的化学性质后,某兴趣小组进行了如下实验:将足量镁条加入到氯化铁溶液中,观察到镁条表面有气泡产生,一段时间后,有黑色固体粉末生成。 【提出问题】产生气体是什么物质? 【作出猜想】猜想一:可能是氯气;猜想二:可能是氢气;猜想三:可能是二氧化碳。 【交流讨论】大家思考后,一致认为猜想三不合理,其理由是_______________________。 【实验与结论】
【继续探究】用pH试纸测得氯化铁溶液pH约为2,说明氯化铁溶液中含有较多的________离子。 65.(2013.咸宁市)金属及金属材料在生产、生活中应用广泛。 (1)铜可以拉成铜丝,这是利用金属的_________。 (2)铝具有很好的抗腐蚀性能,原因是____________________(用化学方程式表示)。 (3)小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):  ①将铁片插入硫酸铜溶液中,铁片表面的现象是_____________________; ②将铜片插入硝酸银溶液中,反应的化学方程式是__________________。 此探究实验的目的是________________________________。 66.(2013.上海市)人类常从矿石中获取金属材料。 (1)铁是冶炼最多的金属。工业炼铁主要反应的化学方程式是3CO+ Fe2O3 (2)铜是人类利用较早的金属,木炭与氧化铜反应生成二氧化碳的化学方程式是___________,反应后固体的质量_____________(填“增大”、“减小”或“不变”) (3)铝在现代生活中得到广泛的应用。炼铝原料水铝石的主要成分是Al(OH)3,Al(OH)3由________种元素组成,2mol Al(OH)3中含有_____g氧元素。 (4)金属冶炼通常使矿石中金属元素转变为_______(填“化合”或“游离”)态。 67.(2013.日照市)(5分)已知材料:在实验室里,金属钠保存在煤油中。在烧杯中加一些水,滴入几滴酚酞试液,然后把一小块钠放入水中,钠与水剧烈反应,钠熔为小球并在水面快速游动,产生一种可燃性气体,烧杯中的液体变红。 请回答下列问题: (1)钠、煤油、水三者的密度大小顺序为 > > 。 (2)钠与水反应的化学方程式为 , 此反应的基本类型是 。 68.(2013.泉州市)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程: 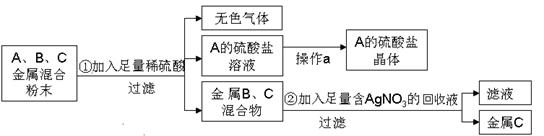 (1) A、B、C三种金属的活动性顺序为 > > 。 (2)金属C是 ,操作a的名称是 。 (3)已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式: 。 69.(2013.泸州市)A、B、C、D为金属活动顺序表中常见的四种金属。已知:①A+BSO4=ASO4+B ②C+H2SO4=CSO4+H2↑ ③B+2DNO3=B(NO3)2+2D 请完成以下填空: (1)金属C在金属活动顺序表中排在氢 (填“前面”或“后面”)。 (2)根据上述反应能判断出其中三种金属的活动性,其金属活动性由强到弱的顺序是____ (用字母填写)。 (3)若A、B、C、D分别为锌、铁、铜、银中的一种,金属C与H2SO4反应后所得溶液呈浅绿色,则金属A为 ,反应③的化学方程式为 。 70.(2013.庆阳市)(1)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残存很少,这说明金、铜、铁这三种金属的活动顺序由强到弱的顺序是 铁、铜、金 ; (2)生铁和钢是世界上用量最大的 (填“金属材料”或“合成材料”);炼铁的原理是利用一氧化碳与氧化铁反应,反应的化学方程式为 。写出防止铁生锈的一种方法是 。 参考答案: 51~57 ADDBDBA 58.(1)水 (2)烤蓝 (3)硫酸镁 硫酸铜 Fe + CuSO4 = FeSO4 + Cu 59.(1)导电 (2)氧气和水 (3)3CO+ Fe2O3 (4)稀盐酸(或稀硫酸或硫酸铜溶液等) 60.⑴水、氧气;涂油;Fe2O3+6HCl=2FeCl3+3H2O ⑵Fe2O3+3CO高温2Fe+3CO2 节约有限的金属资源 61.(1)C (2)Fe + CuSO4 = FeSO4 + Cu (3)①过滤 ②Zn + H2SO4 = ZnSO4 + H2↑ ③AC 62.(1)没有 (2)Al( NO3) 3、Zn( NO3)2、Cu(NO3 ) 2 (3)Cu + 2 AgNO3 = Cu (NO3) 2 + 2 Ag Zn +2AgNO3 = Zn(NO3)2 +2Ag[或 Zn + Cu(NO3)2= Zn(NO3)2 +Cu] 63.⑴铜;硫酸锌⑵向滤渣中加盐酸若有气泡,滤渣为铜和铁,则滤液为硫酸锌和硫酸亚铁;若滤渣中加盐酸无气泡,滤渣为铜,再向滤液中加铁片,有红色固体出现,滤液为硫酸锌和硫酸亚铁、硫酸铜;没有红色固体出现,滤液为硫酸锌和硫酸亚铁。 64. 反应物中不含碳元素,不符合质量守恒定律 带火星的木条没有复燃 水雾 氢 65.(1)延展性 (2)4Al+3O2=2Al2O3(3)①有紫红色的物质生成 ②Cu+2AgNO3=Cu(NO3)2+2Ag 探究铁、铜、银三种金属的活动性顺序 66.(1)Fe2O3(或氧化铁) Fe(或铁) CO2(2)C + 2CuO (3)三 96 (4)游离 67.(1)水 钠 煤油 (2) 2Na+2H2O=2NaOH+H2↑ 置换反应 68.(1)A B C银 蒸发结晶 Mn+ H2SO4 = MnSO4 + H2↑ 69.(1)前面 (2)A>B>D (3)Zn Cu+2AgNO3=Cu(NO3)2+2Ag 70.(1)铁、铜、金 (2)金属材料 3CO+Fe2O3高温 2Fe+3CO2 在铁制品表面镀一层其它金属 (责任编辑:admin) |
