《常见的酸和碱》同步测试(第3课时)
石家庄第41中学 刘 萃
一、选择题
1.下列有关物质的化学式、名称、俗名不完全对应的是( )
A.NaCl 氯化钠 食盐 B.Ca0 氧化钙 熟石灰
C.H2O2 过氧化氢 双氧水 D.NaOH 氢氧化钠 烧碱
考查目的:记忆物质的化学式、名称、俗名。
答案:B。
解析:氧化钙俗名生石灰。
2.物质保存的方法取决其性质。下列药品不需要密封保存的是( )
A.氢氧化钠 B.浓硫酸 C.氯化钠 D.浓盐酸
考查目的:物质的保存方法。
答案:C。
解析:氢氧化钠在空气中会潮解,也会吸收二氧化碳而变质,浓硫酸有吸水性,浓盐酸有挥发性,相对而言氯化钠在空气中比较稳定所以不需要密封保存。
3.下列物质露置于空气中,没有发生化学变化而质量增大的是( )
A.浓硫酸 B.浓盐酸 C.生石灰 D.氢氧化钠
考查目的:物质的性质。
答案:A。
解析:浓硫酸有吸水性,质量会增大但不是化学变化,浓盐酸有量会减小,生石灰会和空气中的水反应生成氢氧化钙,氢氧化钙会和二氧化碳反应,质量增大,氢氧化钠在空气中发生两种变化,潮解是物理变化,吸收二氧化碳是化学变化,质量会增大。
4.下列有关氢氧化钠的描述错误的是( )
A.易溶于水,溶解时放出大量的热 B.对皮肤具有强烈的腐蚀性
C.水溶液能使石蕊试液变红 D.能去油污,厨房清洁剂中含有氢氧化钠
考查目的:氢氧化钠的性质和用途。
答案:C。
解析:氢氧化钠是一种碱,碱性溶液会使石蕊溶液变蓝。
5.工业上广泛用于石油精制、造纸、印染、制肥皂等,则该物质是( )
A.硫酸 B.氢氧化钠 C.熟石灰 D.氯化钠
考查目的:氢氧化钠的用途。
答案:B。
解析:氢氧化钠是一种重要的化工原料。
6.下列气体会污染空气并且可以用氢氧化钠溶液来吸收的是( )
A. CO2 B.O2 C.SO2 D.CO
考查目的:氢氧化钠的化学性质。
答案:C。
解析:氢氧化钠可以和某些非金属氧化物反应,例如二氧化碳、二氧化硫,但不能吸收一氧化碳,本题要求该气体是大气污染物,所以答案是C。
7.下列潮湿的气体,不能用固体氢氧化钠及生石灰干燥的是( )
A.H2 B.CO C.CO2 D.O2
考查目的:氢氧化钠的化学性质。
答案:C。
解析:氢氧化钠和生石灰都可以做干燥剂,但是氢氧化钠和二氧化碳反应,生石灰和水反应的产物氢氧化钙也可以和二氧化碳反应,所以不能用氢氧化钠和生石灰干燥二氧化碳。
8.物质的性质决定它的用途还决定了它的保存方法。固体氢氧化钠具有以下性质:①白色片状固体②有强腐蚀性③易吸收水分而潮解④易溶于水,且溶解放热⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )
A.①② B.①②③ C.②③④ D.③⑤
考查目的:氢氧化钠的性质和用途及其关系。
答案:D。
解析:氢氧化钠固体易吸收水分而潮解,也能与空气中的二氧化碳反应,这些性质决定了氢氧化钠固体必须密封保存。
9.氢氧化钠和氢氧化钙都是常见的碱,下列关于它们的说法中,正确的是( )
A.都能用作建筑材料
B.都能用作某些气体的干燥剂
C.它们的溶液都能用于检验二氧化碳气体
D.它们的溶液都能用于吸收二氧化碳气体
考查目的:氢氧化钠和氢氧化钙的性质和用途。
答案:D。
解析:A项氢氧化钠不能做建筑材料,氢氧化钙可以和沙子混合来砌砖,用石灰浆粉刷墙壁,B项氢氧化钠有吸水性可以做干燥剂,氢氧化钙不能,C项检验二氧化碳应该用澄清石灰水,氢氧化钠虽然可以和二氧化碳反应但是没有明显现象,D项是正确的,但是氢氧化钠溶液吸收效果好。
10.如图所示,将密闭的相互连通的装置放在天平上,调节天平使之平衡。经过一段时间后,下列有关叙述正确的是( )
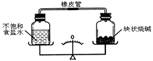
A.指针偏左,食盐溶液一定变稀,烧碱潮解
B.指针偏右,食盐溶液一定饱和,烧碱潮解
C.指针偏左,食盐溶液一定变浓,烧碱潮解
D.指针偏右,食盐溶液一定变浓,烧碱潮解
考查目的:氢氧化钠的性质和溶液。
答案:D。
解析:如图所示,右盘烧碱会吸收食盐水中的水分而潮解,从而质量增大,左盘不饱和食盐水的水分减小,质量减小,质量分数增大,最终指针偏右。
二、填空题
11.实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中二氧化硅缓慢地发生反应,产物使瓶口与瓶塞黏在一起。
反应的化学方程式为SiO2+2NaOH==X+H2O,试推断X的化学式为 。
考查目的:氢氧化钠的性质和质量守恒定律。
答案:Na2SiO3
解析:根据质量守恒定律,反应前后原子种类和数目都不变可以求出该物质的化学式。
12.生石灰是白色的块状物,应用非常广泛。
(1)生石灰的主要成分为 (填化学式)。在食品包装中,常用生石灰做干燥剂,其干燥原理是 (用化学方程式表示);使用时,用纸袋装着生石灰放入食品包装盒中,如果用塑料袋装生石灰就起不到干燥的作用,原因是 。
(2)在农村,生石灰也常用于畜禽栏舍的消毒。畜禽出栏后,将生石灰用水调成20%的石灰乳,涂刷墙面和地面。某农户误将生石灰直接撒在猪圈中消毒,一段时间后发现猪的蹄部干燥开裂,有的甚至出现灼烧,溃疡,原因是 。
(3)上述用的消毒的浆状物要现配现用,放置过久就没有消毒的作用了,其原因是 (用化学方程式表示)
考查目的:生石灰的化学性质。
答案:(1)CaO CaO+H2O=Ca(OH)2 塑料袋有隔潮防水的作用,用塑料袋包装生石灰后,生石灰就不能吸收水分
(2)生石灰与水反应时放出大量的热,将猪蹄灼烧致伤
(3)Ca(OH)2+CO2=CaCO3↓+H2O。
解析:氧化钙俗名生石灰,可以和水反应生成熟石灰,并且该反应会放出大量热。
13.某实验小组取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂。小军认为生石灰已经变质,试剂瓶中可能含有CaO、 Ca(OH)2 、CaCO3等三种物质,并开展如下探究:
实验操作
|
实验现象
|
结论
|
取试样加入水中,充分搅拌
|
产生白色浑浊
|
一定含有CaCO3
|
取试样加入稀盐酸中
|
产生无色气泡
|
一定含有CaCO3
|
请回答:(1)比较甲乙两个方案,你认为那个方案不够合理 ,理由是 。
(2)小红认为放置时间过长可能全部变成了CaCO3,请你利用实验验证小红的猜想 。(3)小林认为不可能全部变成CaCO3,还有CaO,请你利用实验验证小林的猜想 。
考查目的:生石灰变质的探究。
答案:(1) 甲 Ca(OH)2微溶于水,在水中也会产生白色浑浊 (2) 取试样于试管中加入水,充分振荡后过滤,向滤液中滴加酚酞,观察,若为无色,则试样已全部变成了CaCO3
(3)取试样于试管中加入水,充分振荡,触摸试管外壁,若温热,过滤,向滤液中滴加酚酞,观察,若溶液变红,可证明试样中含有CaO。
解析:本题属于成分探究类型的的题目。探究是否含有某成分,关键是把握该物质主要的化学性质。全部变质成为碳酸钙,意味着没有了氧化钙和氢氧化钙,只要能证明加入水后的滤液不再是碱性即可。若要证明还有氧化钙,则可利用氧化钙和水反应放热这一事实。
(责任编辑:admin) |

