|
九年级化学上册期末测试 湖北省枣阳市兴隆二中 丁照明 程 云 可能用到的相对原子质量:C-12 H-1 N-14 P-31 O-16 K-39 S-32 Cl-35.5 Mn-55 一、选择题(每小题2分,共40分) 1.下列现象中发生化学变化的是( ) A、纸张燃烧 B、玻璃破碎 C、冰雪融化 D、酒精挥发 2.下列化学实验操作,正确的是( ) 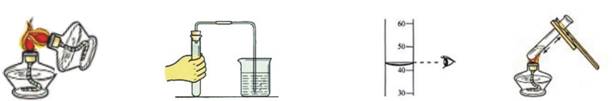 A、点燃酒精灯 B、检查气密性 C、读取液体体积 D、加热液体 3.下列符号既可表示一个原子,又可表示一种元素,还能表示一种物质的是( ) A、H2 B、2N C、Cu D、O 4.一氧化氮是汽车尾气中的一种大气污染物,它是一种无色气体,难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体,在实验室中收集一氧化氮可采用的方法是( ) A、排水集气法 B、向上排空气法 C、向下排空气法 D、向上排空气法或排水集气法 5.除去CO中混有的少量CO2,应把混合气体通过( ) A、少量的水 B、灼热的氧化铜 C、澄清的石灰水 D、点燃 6.造成酸雨的主要物质是( ) A、甲烷和一氧化碳 B、二氧化硫和一氧化碳 C、一氧化碳和二氧化碳 D、二氧化硫和二氧化氮 7.在化学反应中,一定发生变化的是( ) A、原子种类 B、分子种类 C、元素种类 D、分子数目 8.下列是几种粒子的结构示意图,其中表示阳离子的是( ) 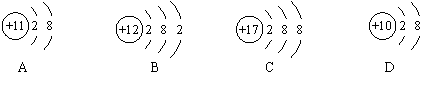  9.右图是某反应的微观示意图,“ 9.右图是某反应的微观示意图,“A、乙中含有四种元素 B、反应前后分子个数不变 C、反应的本质是原子进行了重新重合 D、甲、乙相对分子质量和等于丙、丁相对分子质量之和 10.“八月桂花香”这一现象说明( ) A、分子很小 B、分子分裂成原子 C、分子在不断地运动 D、分子之间有间隔 11.下列物质中含有氧气的是( ) A、二氧化锰 B、氯酸钾 C、氯化镁 D、空气 12.下列对分子、原子、离子的认识,正确的是( ) A、分子是保持物质性质的最小粒子 B、原子是最小粒子,不可再分 C、原子得到或失去电子后形成离子 D、分子可以构成物质,原子不能构成物质 13.下列物质的用途,既利用了物理性质,又利用了化学性质的是( ) A、木炭作燃料 B、制糖工业中用活性炭来脱色以制白糖 C、CO2用来灭火 D、干冰用于人工降雨 14.“生命可贵,安全第一”下列采取的安全措施错误的是( ) A、晚上煤气泄漏,立即开窗通风 B、点燃氢气前,应先检验氧气的纯度 C、用煤炉取暖,在煤炉上放一壶水以防止煤气中毒 D、进入久未开启的菜窑,先用蜡烛做灯火实验 15.对下列实验操作指定容器中的水,其解释没有体现水的主要作用的是( )
16.“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊溶液中,然后再加热,溶液颜色变化是( ) A、先变蓝后变紫 B、变红后颜色不再改变 C、先变无色后变红色 D、先变红色后变紫色 17.空气中含量高且化学性质不活泼的气体是( ) A、氮气 B、氧气 C、二氧化碳 D、稀有气体 18.物质在氧气中燃烧的实验现象描述正确的是( ) A、木炭:产生蓝色火焰 B、铁丝:发出耀眼的白光 C、镁带:火焰呈淡蓝色 D、硫粉:产生明亮的蓝紫色火焰 19.某物质经分析只含有一种元素,则该物质不可能是( ) A、混合物 B、纯净物 C、单质 D、氧化物 20.鉴别H2、CO、CH4三种气体,下列说法正确的是( ) A、通过灼热的氧化铜 B、闻气味 C、点燃后看发出火焰焰色 D、检验燃烧的产物 二、填空题(每空1分,化学方程式2分共39分) 1.用化学符号填空: 两个氢原子_______;干冰_______;锌离子_______;硝酸铁_______;乙醇_______;氧化镁中镁元素的化合价为+2价______。 2.请以氢气、氮气、氧气、二氧化碳、二氧化硫等五种气体中,按要求将相应物质的化学式填写在题中的空白处。 (1)属于空气污染物的气体是_______; (2)能支持燃烧的气体是_______; (3)焊接金属时常用作保护气的是_______; (4)绿色植物光合作用吸收的气体是_____。 3.2009年4月以来高致病性甲型H1N1流感呈现出在全球蔓延的趋势,根据世界卫生组织报道,目前尚无法专门针对人类感染H1N1流感的特效药,但推荐使用“达菲”胶囊,根据“达菲”的化学式C16H31N2PO8,从化学的角度分析,你能获得的信息有: ①_________________________________ ;②_________________________________。 4.随着经济的发展,能源与环境成为人们日益关注的问题。 (1)煤、________和__________常称为化石燃料。 (2)煤发电时,将煤块粉碎成煤粉,其目的是_____________________________________。 (3)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体,为减少它的排放,科学家致力研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷,该反应的化学方程式为: __________________________________。 (4)下列措施中,有利于降低大气中的二氧化碳含量的是( ) A、大量使用化石燃料 B、植树造林,增大植被面积 C、将二氧化碳变废为宝,循环利用 5.化学知识在生产生活中有广泛的应用 (1)时下兴起的环保炭雕工艺品,是以活性炭为原料,采用传统手工雕刻而成,炭雕工艺品既能装饰居室,又对甲醛等有害气体具有很强的____________作用,能有效地净化室内空气。 (2)通常所说的煤气中毒是指_______________(填化学式)引起的中毒。 (3)长期使用的热水瓶内胆常有一层水垢(主要成分是碳酸钙),可以用稀盐酸除去,反应的化学方程式为_______________________。 (4)为防止彩色照片褪色,可将照片用塑料薄膜封闭,目的是_______________________。 (5)为保证安全,凡是可燃性气体,点燃前都要检验气体的__________。 (6)不经常使用的锁,可向锁眼中加入少量铅笔芯粉末,以容易开启,这是因为_______________________________。 6.黑火药是我国四大发明之一,黑火药的爆炸可用以下式子表示其反应和生成物:2KNO3+3C+S  7.A、B、C、D、E各代表木炭、氧气、一氧化碳、二氧化硫、氧化铜中的一种,一定条件下,相连环物间能发生反应(如右图),则: 7.A、B、C、D、E各代表木炭、氧气、一氧化碳、二氧化硫、氧化铜中的一种,一定条件下,相连环物间能发生反应(如右图),则:(1)下列物质的化学式分别是:A________;B________;C________;D________。 (2)我能写出其中的一个化学方程式:__________________________。 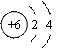 8.碳与碳的化合物在工农业生产及日常生活中有广泛的用途: 8.碳与碳的化合物在工农业生产及日常生活中有广泛的用途:(1)右图是碳原子结构示意图,碳原子的质子数是________,碳元素在元素周期表中位于第______周期。 (2)古代用墨书写或绘制的字画虽年久仍不变色,原因是墨中主要成分碳在常温下具有______性。 (3)二氧化碳能参与光合作用完成大气中的“碳循环”,但是大气中的二氧化碳的含量不断上升,会使全球变暖,从而导致_____________。蔬菜、大棚用作“气肥”的二氧化碳,可用多种方法制得,例如可以用稀硫酸(H2SO4)与碳酸氢铵(NH4HCO3)反应制得,反应后生成硫酸铵,水和二氧化碳,该反应的化学方程式为______________________ 三、实验探究题(每空1分,化学方程式2分共12分) 实验室制取气体的装置如下图所示,根据所学知识,回答下列问题: 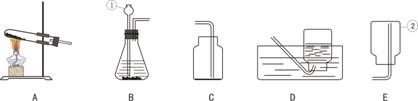 (1)图中标有①②的仪器名称:①____________;②_____________。 (2)写出用装置A制取氧气的一个化学方程式______________________;A装置中试管口略向下倾斜的目的是____________________________。 (3)某同学用C装置集满一瓶氧气后,实验时发现氧气不纯,原因可能是____________。 (4)实验室用石灰石和稀盐酸反应制取二氧化碳时,应选用图中__________和__________来组装一套实验装置,检验二氧化碳集满的方法是______________________________。 (5)实验室用锌粒与稀硫酸在常温下反应制取氢气,需选用的发生装置为__________,收集装置为___________。 四、计算题(3+6) 1.尿素是一种优质的氮肥,其化学式为CO(NH2)2,据此我能计算: (1)尿素的相对分子质量为__________。 (2)一袋50 kg的尿素中氢元素的质量是________kg(保留一位小数) 2.某同学取氯酸钾和二氧化锰混合物15.5 g,加热至完全反应得到10.7 g固体,问10.7 g固体中有哪些物质,各有多少克? 参考答案: 一、选择题
二、填空题 1、2H;CO2;Zn2+ Fe(NO3)3 C2H5OH;;2、SO2;O2;N2;CO2; 3、①达菲是由C、H、N、P、O五种元素组成的;一个达菲分子是由16个碳原子、31个氢原子、2个氮原子、1个磷原子、8个氧原子构成的。 4、(1)石油;天然气;(2)增大与氧气的接触面积;(3)CO2+4H2 5、(1)吸附;(2)CO;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;(4)隔绝空气;(5)验纯;(6)铅笔芯中含有石墨,石墨具有润滑性; 6、CO2;202:36:32 7、(1)A、CO2 B、C C、CuO D、O2 (2)CuO + CO 8、6;二;稳定;温室效应;H2SO4+2NH4HCO3=(NH4)2SO4+2H2O+2CO2↑ 三、实验探究题 (1)①长颈漏斗;②集气瓶(2)2KMnO4 四、计算题 1、(1)60(2)23.3 2、解:10.7 g固体中含有氯化钾和二氧化锰。 根据质量守恒定律生成氧气的质量为:15.5 g-10.7 g=4.8 g 设生成氯化钾的质量为x 2KClO3 149 96 x 4.8 g 149/96=x/4.8 g x=149*4.8g/96=7.45 g 则剩余固体中MnO2的质量为:10.7 g-7.45 g=3.25 g 答剩余固体中含有氯化钾7.45 g,含有二氧化锰3.25 g (责任编辑:admin) |

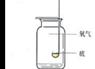 硫在O2中燃烧
硫在O2中燃烧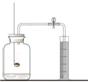 测定空气中O2含量
测定空气中O2含量