|
初中化学1~5单元化学用语竞赛试题 湖北省宜昌市十六中学 冯敏敏 说明:本试卷试题若没有特殊说明,请用化学用语答题 相对原子质量:C—12 O—16 H—1 一、我会书写 1、两个氮原子 2、3个铝离子 3、4个五氧化二磷分子 4、2个氢氧根离子 5、氧化铁中铁元素的化合价 6、氯气 7、2个钠离子 8、硫酸根离子 9、n 个亚铁离子 10、负2价的硫元素 11、空气中的主要气体 12、空气中含量最多的元素 13、生物细胞中含量最多的物质 14、地壳中含量最多的非金属元素和金属元素组成的化合物 15、能导电的一种单质 16、 是生命之源 17、 等气体可用作多用途的电光源 18、能造成酸雨的一种气体 19、写出电解水的化学方程式 该反应中不变的最小粒子是 ,发生了变化的粒子是 ;保持水的化学性质的是 ,该反应的类型是 20、物质是由粒子构成的,例如:由分子构成的一种单质 ;一种化合物 由原子构成的一种物质 ;由离子构成的一种物质 。 21、密度最小的一种气体 ; 22、常用来充灌飞艇的气体是 ; 23、 物质在空气中和在氧气中燃烧的火焰颜色不同 24、碳酸钙是由 元素组成的。 25、硝酸铵的化学式为 ,并标出氮元素的化合价 二、我会分析 26、小民同学在化学晚会上进行化学用语接龙活动,请你也参与 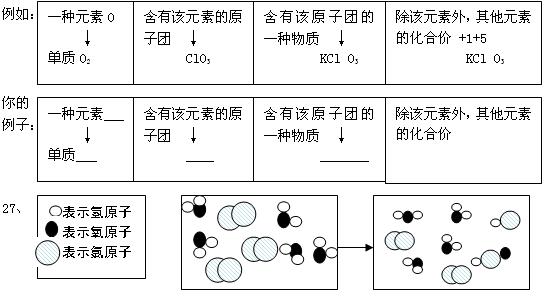 根据上图,你写出的化学方程式为 28、氯气和氧气一样,都是活泼的非金属单质。甲烷和氧气反应的化学方程式为: CH4+2O2 29、已知反应 ;2X+5O2 30、化学方程式□CO+□Fe3O4 31、2003年10月15日,中国“神州5号”飞船载人航天取得成功,偏二甲肼是火箭推进器的常用燃料。根据偏二甲肼的化学式C2H8N2,你知道的信息有:请写三点 ① ② ③ 32、下列关于“2”的含义的解释中,正确的是:( ) A、Zn2+中的“2+”表示锌粒带有2个单位的正电荷 B、2NO中的“2”表示2个一氧化氮分子 C、H2SO3中的“2”表示一个亚硫酸分子中含有两个氢元素 D、Al2 33、在2H+、2CO、2O、2Ca2+、2NH3等符号中,能够表示2个分子的符号有() A、1个 B、2个 C、3个 D、4个 三、我会说明 34、到目前为止,我们已学过很多不同的化学反应。请举例说明: ⑴有水生成的分解反应: ⑵有水生成的化合反应: ⑶有氧气生成的分解反应: ⑷有氧气生成的化合反应: ⑸反应物为白色的分解反应: ⑹生成物为白色的化合反应:① ② ⑺生成物为黑色的化合反应: ⑻有二氧化碳生成的分解反应: ⑼有二氧化碳生成的化合反应: ⑽有二氧化碳生成的氧化反应: ⑾有二氧化锰生成的分解反应: ⑿二氧化锰作为该反应催化剂的化学反应: 35、日常生活中的很多现象,都需要我们用化学知识来解释,例如: ⑴我们长跑后,腿会发酸,这是因为肌肉中产生了乳酸C3H6O3,过一段时间后,这种酸痛现象会慢慢消失,原因是乳酸与人体中的氧气反应生成了水和二氧化碳,该反应的化学方程式为: ⑵向澄清的石灰水【主要成分为Ca(OH)2】中吹气,石灰水会变浑浊,原因是氢氧化钙与二氧化碳反应生成了水与碳酸钙沉淀。该反应为 ⑶如果将一块普通的棉布浸在氯化铵的饱和溶液中,片刻之后,取出晾千就成防火布了。将这块经过氯化铵浸泡处理的布用火柴点,不但点不着,而且还冒出白色的烟雾。你知道,这是为什么吗?原来,经过这种化学处理的棉布(防火布)的表面附满了氯化铵的晶体颗粒,氯化铵这种化学物质的热稳定性很差,受热后会发生分解,分解出两种不能燃烧的气体,一种是氨气,另一种是氯化氢气体。该反应的原理为 这两种气体把棉布与空气隔绝起来,棉布在没有氧气的条件下当然就不能燃烧了。当这两种气体保护棉布不被火烧的同时,它们又在空气中相遇,重新化合而成氯化铵小晶体,这些小晶体分布在空气中,就象白烟一样。实际上,氯化铵这种化学物质是很好的防火能手,戏院里的舞台布景、舰艇上的木料等,都经常用氯化铵处理,以求达到防火的目的。 ⑷泡沫灭火器内有两个容器,分别盛放两种液体,它们是硫酸铝和碳酸氢钠溶液,两种溶液互不接触,不发生任何化学反应。(平时千万不能碰倒泡沫灭火器)当需要泡沫灭火器时,把灭火器倒立,两种溶液混合在一起,就会产生大量的二氧化碳气体、硫酸钠和氢氧化铝固体。请你写出该反应的原理: ⑸变色眼镜是如何变色的?制造变色眼镜的镜片玻璃中,除了一般原料外,还要加入适量的溴化银AgBr和氧化铜的微小晶粒,做成镜片后,其中的溴化银受强光照射时会分解为银和溴Br2,该反应为: 因为银的微粒呈深色,所以镜片颜色就变深。当光线变暗(弱)时,银和溴在催化剂氧化铜的作用下,又重新化合生成溴化银,该反应为: 于是镜片的颜色又变浅了。 ⑹1855年,瑞典人设计制造出了世界上第一盒安全火柴。安全火柴在火柴盒外侧涂上红磷,火柴头上有氯酸钾和三硫化二锑这两种引火药。当你擦火柴时,火柴头蹭下的一丁点儿红磷,由于摩擦生热,达到着火点,起火了。火星引着三硫化二锑,氯酸钾受热放出氧气,帮助燃烧得更旺。火柴杆是用松木或白杨木做的,前端又浸透了石蜡和松香,使火柴擦着后,火焰容易烧到火柴杆上去,发火的时间也长一些。 请写出其中你熟悉的两个化学反应的方程式: 、 (责任编辑:admin) |
