|
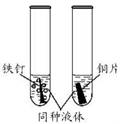
一、选择题 1.铝在一百多年里产量得到大幅度的提高,并被广泛地使用,原因之一就是铝的抗腐蚀性能好。铝具有良好抗腐蚀性能的原因是( ) A.铝的化学性质不活泼 B. 铝表面生成一层致密的氧化铝保护膜 C.铝常温下不与氧气反应 D. 铝不与酸、碱反应 考查目的:铝的抗腐蚀性能 答案:B。 解析: 铝的化学性质比较活泼,在空气中和氧气发生缓慢氧化,表面生成一层致密的氧化铝保护膜,从而阻止铝进一步氧化。 2.某金属放入稀硫酸中,不产生气泡,该金属可能是( ) A.铝 B.铜 C.镁 D.铁 考查目的:金属和稀硫酸的反应现象 答案:B。 解析:铝、镁、铁都可以和稀硫酸反应生成氢气,而铜不可以和稀硫酸反应生成氢气。 3.由下图信息可知,金属活动性最不活泼的是 ( )  A.镁 B.锌 C.铁 D.铜 考查目的:金属和稀硫酸反应的现象 答案:D。 解析:根据金属是否和稀硫酸反应生成氢气以及产生气体的快慢可以判断金属活动性强弱,由图中现象可知金属活动性强弱顺序如下:镁〉锌〉铁〉铜。 4. 下列关于锌、铁、铜的说法错误的是( ) A.均可以导电 B.均可以和氧气反应 C.均可以和稀盐酸反应 D.铁能与硫酸铜溶液的溶质发生置换反应 考查目的:金属的性质 答案:C。 解析:C项铜不可以和稀盐酸反应。 5. 下列现象和事实,可用金属活动性作出合理解释的是( ) ①金属镁在空气中比铝更易点燃,说明镁比铝活动性强; ②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强; ③硫酸铜、石灰水配制农药波尔多液,不宜用铁制容器; ④金属锌与稀硫酸反应速率适中,更适于实验室制取氢气。 A.①② B.③④ C.①③④ D.①②③④ 考查目的:金属的化学性质 答案:C。 解析:①金属与氧气的难易以及剧烈程度也能=反应金属的活动性,②铝的化学性质比较活泼,在空气中和氧气发生缓慢氧化,表面生成一层致密的氧化铝保护膜,从而阻止铝进一步氧化,所以铝的抗腐蚀性能比较好,③铁可以和硫酸铜溶液发生反应,所以不宜用铁制容器配制波尔多液,④金属锌与稀硫酸反应速率适中,更适于实验室制取氢气。正确的是①③④。 6.将一枚洁净的铁钉浸入稀硫酸中,下列叙述中正确的是( ) ①铁钉表面产生气泡 ②液体由无色逐渐变为浅绿色 ③铁钉的质量减轻 ④液体的质量减轻 A.②③ B.①②④ C.①②③ D.①②③④ 考查目的:铁和稀硫酸反应的现象 答案:C。 解析:铁和稀硫酸反应生成氢气和硫酸亚铁,硫酸亚铁溶液呈浅绿色,根据质量守恒可以看出铁钉质量减轻,溶液质量增加,所以C正确。 7.(2013年陕西省)下列有关实验现象描述不正确的是 ( )  A.细铁丝在空气中剧烈燃烧 B.蜡烛逐渐熄灭
将该金属投入稀盐酸中,可产生大量的无色气体。根据上述信息回答以下问题: (1)试推断该金属的一种用途____________________________; (2)该金属的活动性比铜__________________________(填“强”或“弱”); (3)请自选试剂,设计实验探究该金属与铁的活动性强弱,并完成下表:
考查目的:金属的性质和用途及活动性顺序 答案:(1)做导线 (2) 强 (3) 活动性比铁强 将该金属表面打磨后伸入硫酸亚铁溶液中 金属表面有一层黑色固体附着 该金属活动性强于铁 解析: 金属的性质决定用途,利用金属和盐溶液的置换反应可以验证金属的活动性 13.(2013年咸宁市)金属及金属材料在生产、生活中应用广泛。 (1)铜可以拉成铜丝,这是利用金属的_________。 (2)铝具有很好的抗腐蚀性能,原因是____________________(用化学方程式表示)。 (3)小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):  ①将铁片插入硫酸铜溶液中,铁片表面的现象是_____________________; ②将铜片插入硝酸银溶液中,反应的化学方程式是__________________。 此探究实验的目的是________________________________。 考查目的:金属的性质及活动性顺序 答案:(1)延展性 (2)4Al+3O2=2Al2O3(3)①有紫红色的物质生成 ②Cu+2AgNO3=Cu(NO3)2+2Ag 探究铁、铜、银三种金属的活动性顺序 解析:利用金属和盐溶液的置换反应可以验证金属的活动性。 (责任编辑:admin) |