|
1.(2013.佛山市)以下说法正确的是 ( ) A.溶液一定是均一、无色、稳定的 B.均一、稳定的液体一定是溶液 C.溶液的溶质一定是固体 D.溶液一定是混合物 考查目的:对溶液概念的准确理解和把握。 答案:D。 解析:A项溶液不一定是无色的,例如KMnO4溶液是紫色的,CuSO4溶液是蓝色的,故A项错误;B项均一、稳定的液体不一定是溶液,例如水、酒精;C项溶质可以是气体、液体和固体;D项根据溶液的定义,溶液是“一种”或“几种物质”分散到另一种物质里形成的,其中至少涉及到两种物质混合在一起,因此是混合物。 2.(2013?滨州)关于溶液和乳化的下列说法这种错误的是 ( ) A. 溶液中可以含有多种溶质 B. 溶液是均一、稳定的混合物 C. 用汽油洗去衣服上的油污是乳化现象 D. 溶液不一定是无色的 考查目的:对溶液和乳化概念的准确理解。 答案:C。 解析:C项用汽油洗去衣服上的油污溶解现象 3.30ml水和70ml酒精混合,下列说法正确的是 ( ) A.溶质是水,溶剂是酒精 B.形成均一、稳定的溶液形后酒精分子停止运动 C.混合后溶液的体积是100ml D.混合后溶液的质量等于溶质的质量和溶剂的质量之和 考查目的:物质溶解时吸热、放热现象溶质、溶剂、溶液的关系。 答案:D。 解析:两种液体混合,如果其中有一种是水,无论体积多少,水为溶剂,故A项错误;B项达到均一状态后,分散在溶剂中的溶质分子或离子仍然处于不停地无规则运动状态之中,B项错误;C项两种液体混合,由于微粒间有间隔,体积不等于二者体积之和,故C错误;D项溶液由溶质和溶剂两部分构成,故溶液质量等于溶质质量和溶剂质量之和。 4.(2011.苏州市)将适量的下列物质溶解于水的过程中,会使溶液的温度显著降低的是 ( ) A.氢氧化钙 B.硝酸铵 C.氢氧化钠 D.蔗糖 考查目的:物质溶解时吸热、放热现象。 答案:B。 解析:NaOH溶于水放热,溶液温度升高;NH4NO3溶于水吸热,溶液温度降低;蔗糖和氢氧化钙溶于水吸放热现象不明显,溶液温度几乎不变。 5.将适量的下列物质放入水,因溶解而使溶液温度显著升高的是 ( ) A. 氧化钙 B.氢氧化钙 C.氢氧化钠 D.硝酸铵 考查目的:物质的溶解伴随有热量的变化,化学反应中伴随热量变化。 答案:C。 解析:物质的溶解伴随有热量的变化,多数物质溶于水热量没有变化,溶解放热的典型物质是氢氧化钠,溶解吸热的典型物质是硝酸铵。A氧化钙放入水中放热,不是氧化钙溶于水放热,而是氧化钙与水反应放热,故答案是C。 6.小明在玻璃片上滴几滴水,往右图所示的烧杯中加入一种物质,轻轻搅拌后,烧杯和玻璃片粘在一起。加入的物质可能是 ( ) 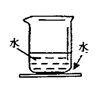 A.食盐 B.硝酸铵 C.氧化钙 D.硝酸钾 考查目的:物质溶解时吸热、放热现象。 答案:B。 解析:烧杯中加入硝酸铵,硝酸铵溶于水吸热,温度降低玻璃片上的水遇冷结冰,使烧杯和玻璃片黏在一起,故答案是B。 7.小明设计了如下图所示的装置A、B进行趣味实验。 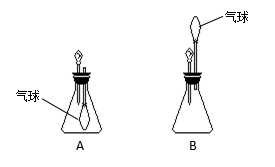 (锥形瓶和滴管中分别盛放不同物质) 使用装置A进行实验时,将滴管中的物质加入到锥形瓶中,发现气球鼓,则锥形瓶中的物质,滴管中的液体物质可能为 ( ) ①石灰石和稀盐酸 ②镁和稀盐酸 ③硝酸铵和水 ④氢氧化钠和水 A.①② B.①②④ C.③ D.④ 考查目的:反应现象和本质的联系;物质溶解时吸热、放热现象。 答案:C 解析:(1)使用装置A进行实验时,将滴管中的物质加入到锥形瓶中,发现气球鼓起,则锥形瓶中压强小于瓶外大气压,因此可能是瓶内气体被滴管中的液体反应生成物中没有气体,也可能是瓶内物质与滴管中物质作用,使瓶内温度降低,①②均生成气体瓶内压强大于瓶外压强,④氢氧化钠溶于水放热同样使瓶内压强大于瓶外压强,③NH4NO3溶于水,,使瓶内的压强小于瓶外压强,故③正确。 8.50克食盐,放入100克水中,溶解了36克,则关于食盐溶液的下列说法中不正确的是 ( ) A.溶质的质量是50g B.溶液的质量是136克 C.配制溶液时,搅拌可以增大氯化钠的溶解速度 D.氯化钠溶于水溶液温度几乎不变 考查目的:溶液的概念、溶质、溶剂、溶液的关系。 答案:A 解析:溶液由溶质和溶剂两部分组成,只有溶解的部分才是溶质,未溶解的部分不在溶液中,因此溶液中溶质的质量是36克,故A项错误, 二、填空题 1.按下图所示装置进行实验。向小试管中分别加入适量的下列固体物质溶于水,右侧U形管中滴有红墨水的液面发生明显变化,请在下表的空白处填写U型管中液面会发生的变化。 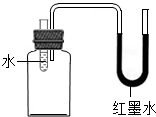
考查目的:溶解时吸热、放热现象。 答案:
解析:硝酸铵溶于水吸热,广口瓶内液体温度降低,广口瓶内气体降温体积减小,广口瓶内压强小于瓶外压强,U型管右侧液面降低;氢氧化钠溶于水放热,试管内液体温度升高,广口瓶内气体升温体积增大,广口瓶内压强大于瓶外压强,U型管右侧液面升高;氯化钠溶于热量几乎不变,试管内液体温度不变,广口瓶内气体体积不变,广口瓶内压强不变,,U型管右侧液面不变。 2.6.5克锌与100克稀硫酸混合,得到无色溶液。 (1)若二者恰好完全反应,则在100克稀硫酸中溶质的化学式为 ,其质量为 g,溶剂的的化学式为 ,其质量为 g,完全反应后,所得溶液的质量为 g,其中溶质的化学式为 ,其质量为 g,溶剂的的化学式为 ,其质量为 g。 (2)若锌完全反应,则所得溶液中溶质的化学式为 。 考查目的:溶液的概念、溶质、溶剂、溶液的关系。 答案:(1)H2SO4 9.8 H2O 90.2 106.3 ZnSO4 16.1 H2O 90.2 (2)ZnSO4 或ZnSO4和H2SO4 解析:,稀硫酸是溶液,其中的溶质是硫酸,溶剂是水,锌与硫酸反应,与水不反应。根据化学方程式计算相关物质的质量。 Zn + H2SO4 = ZnSO4 + H2↑ 65 98 161 2 6.5g x y z 解得: x=9.8g y= 16.1g z= 0.2g 故100g稀硫酸中溶质H2SO4的质量为 9.8g,溶剂水的质量为 100g-9.8g=90.2g 根据质量守恒定律,反应后所得溶液质量为 6.5g+100g-0.2g=106.3g,其中溶质为ZnSO4 的质量为16.1g,溶剂质量的质量不变,为 90.2g。 (责任编辑:admin) |
